В современной стандартизации лекарственного сырья и препаратов, в фармацевтическом анализе актуальными являются подбор, совершенствование и разработка современных и специфичных методик определения подлинности и качества, отвечающих требованиям валидации и соблюдению системного подхода в ряду «сырьё – препарат» [7].
Для продукта пчеловодства – сырья прополиса, имеющего широкий ареал сырьевой базы [1–4, 6], включенного в государственный реестр лекарственных средств РФ [5] и являющегося источником эффективных и безопасных антибактериальных и регенерирующих лекарственных средств [1, 3, 4, 6, 8, 9], ранее были разработаны современные и специфичные подходы к стандартизации [1–4, 6].
Фармакологическая активность препаратов прополиса обусловлена компонентным составом биологически активных соединений (БАС), который как по литературным данным, так и по результатам наших исследований близок к составу тополя почек, но вариабелен и определяется химическим составом преобладающих растительных источников (тополь и др.) [1–4, 6, 8–10]. Популярным лекарственным средством является «Прополиса настойка» (рег. № 90/111/3, Фармакопейная статья (ФС) 42-3736-99) [5, 6].
Актуальна проблема совершенствования фармакопейного анализа для лекарственных средств на основе прополиса, в случае которых стандартизация недостаточно специфична и современна – осуществляется без использования стандартного образца, а методики не в полной мере отвечают параметрам валидации и системного подхода в ряду «сырье – лекарственное средство» [1–4, 6, 7, 9].
Цель исследования ‒ разработка методик определения подлинности и количественного определения биологически активных соединений прополиса настойки.
Материал и методы исследования
Были исследованы серийные образцы лекарственного средства «Прополиса настойка» российских производителей, представленные в табл. 1.
Таблица 1
Содержание суммы флавоноидов и фенилпропаноидов в образцах препарата «Прополиса настойка» российских производителей
|
Номер образца |
Наименование производителя (серия) |
Содержание флавоноидов и фенилпропаноидов, (%) |
|
1 |
ОАО «Татхимфармпрепараты», г. Казань (240709) |
1,98 ± 0,087 |
|
2 |
ООО «Тульская фармацевтическая фабрика», г. Тула (20211) |
1,66 ± 0,073 |
|
3 |
ООО «Тульская фармацевтическая фабрика», г. Тула (91012) |
1,91 ± 0,084 |
|
4 |
ООО «БЭГРИФ», г. Бердск Новосибирской области (030411) |
1,95 ± 0,086 |
|
5 |
ООО «БЭГРИФ», г. Бердск Новосибирской области (090912) |
1,37 ± 0,060 |
|
6 |
ООО «Гиппократ», г. Самара (04112010) |
1,49 ± 0,066 |
|
7 |
ООО «Гиппократ», г. Самара (03072012) |
1,67 ± 0,074 |
|
8 |
ЗАО «Московская фармацевтическая фабрика», г. Москва (210810) |
2,02 ± 0,089 |
|
9 |
ООО «ВАТХЭМ – ФАРМАЦИЯ», г. Рязань (011110) |
1,55 ± 0,068 |
|
10 |
ЗАО «ВИФИТЕХ», Московская область, Серпуховский район, п. Оболенск (040111) |
2,06 ± 0,091 |
|
11 |
ЗАО «ВИФИТЕХ», Московская область, Серпуховский район, п. Оболенск (081012) |
1,58 ± 0,070 |
|
12 |
ОАО «Тверская фармацевтическая фабрика», г. Тверь (130809) |
1,90 ± 0,084 |
|
13 |
ОАО «Тверская фармацевтическая фабрика», г. Тверь (290910) |
1,64 ± 0,073 |
Регистрацию спектров проводили с помощью спектрофотометра «Specord 40» (Analytik Jena AG, Germany) в диапазоне длин волн 190–500 нм.
Результаты исследования и их обсуждение
Исследование электронных спектров поглощения света образцов прополиса настойки исходной и после добавления к 1 мл настойки 1 мл 3 % спиртового раствора алюминия хлорида (AlCl3) с последующим разведением 1:2500 (рис. 1–3), а также дифференциальных (рис. 1.1–3.1) показало, что аналогично сырью прополиса и тополя почек характер суммарных кривых поглощения электронных спектров определяется в основном веществами флавоноидной природы. Общим для электронных спектров всех исследованных образцов является выраженное поглощение света в УФ-области (в интервале от 260 до 330 нм) – основной максимум поглощения спектра находится около 290 ± 2 нм, а после добавления к 1 мл настойки 1 мл 3 % раствора AlCl3 – дает батохромный сдвиг в УФ-область 307 ± 3 нм (флаваноны пиностробин и др.), а в видимой области спектра – 407 ± 10 нм (рис. 1–3 и 1.1–3.1). Большинство спектров образцов прополиса настойки ближе к «тополиному» типу прополиса (образцы № 1–7, 9–11, 13), некоторые – к «смешанному» типу (образцы № 8 и 12). Исходные кривые образцов «смешанного» типа отличаются от других более высоким поглощением в области 320 ± 5 нм.
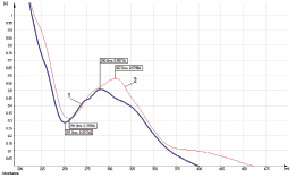
Рис. 1. Спектр раствора образца прополиса настойки № 3. Обозначения: 1 – раствор настойки исходный (разведение 1:2500), 2 – с добавлением к 1 мл настойки 1 мл 3 % спиртового раствора AlCl3 (разведение 1:2500)
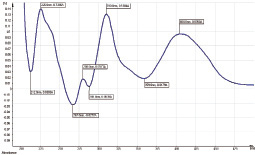
Рис. 1.1. Дифференциальный спектр раствора прополиса настойки № 3 с добавлением к 1 мл настойки 1 мл 3 % спиртового раствора AlCl3 относительно исходного (разведение 1:2500)
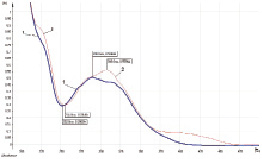
Рис. 2. Спектр раствора образца прополиса настойки № 12. Обозначения те же
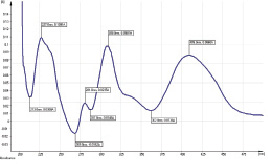
Рис. 2.1. Дифференциальный спектр раствора прополиса настойки № 12
В дифференциальных спектрах (рис. 1.1–3.1) всех исследованных образцов препарата прополиса (после добавки AlCl3 по сравнению с исходным) наблюдаются отчетливо выраженные максимумы поглощения при 225 ± 2, 281 ± 1, 312 ± 3, 407 ± 4 нм. Кроме того, для всех дифференциальных спектров образцов препарата прополиса характерны выраженные минимумы поглощения при 213 ± 1, 266 ± 3, 289 ± 3, 356 ± 3 нм.
В спектре спиртового раствора ГСО пиностробина (рис. 3) присутствуют максимумы поглощения при 213, 289 нм и плечо при 320 нм, минимумы – при 204, 247 нм. После добавления AlCl3 (рис. 3) в спектре наблюдается батохромный сдвиг соответствующих максимумов (222, 308 и 376 нм) и минимумов (212, 255 и 333 нм) поглощения света. Дифференциальная кривая ГСО в целом согласуется с таковыми препаратов прополиса (рис. 3.1).
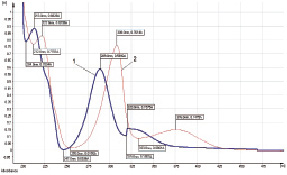
Рис. 3. Спектр спиртового раствора образца пиностробина (разведение 1:125000). Обозначения: 1 – раствор исходный, 2 – с добавлением к 1 мл исходного 1 мл 3 % спиртового раствора AlCl3
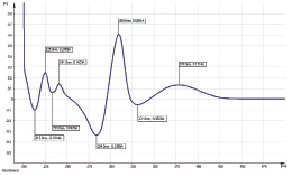
Рис. 3.1. Дифференциальный спектр спиртового раствора пиностробина с добавлением к 1 мл раствора А 1 мл 3 % спиртового раствора AlCl3 относительно исходного (разведение 1:125000)
Предлагаем для усиления подлинности препарата «Прополиса настойка» ввести в нормативную документацию (НД) на сырье и препараты прополиса характеристику электронного спектра как прямого (исходного), так и дифференциального. Электронный спектр сырья прополиса и лекарственного средства «Прополиса настойка» должен иметь выраженный максимум поглощения в области 290 ± 2 нм и выраженный минимум при 252 ± 3 нм. Характерный дифференциальный спектр сырья прополиса и препарата «Прополиса настойка» после добавления раствора AlCl3 должен иметь выраженные максимумы поглощения света: при 225 ± 2, 280 ± 2 нм, при 312 ± 3, 406 ± 3 нм и выраженные минимумы: при 213 ± 1, 267 ± 3, 289 ± 3, 356 ± 3 нм.
В методике количественного определения суммы флавоноидов и фенилпропаноидов в препаратах прополиса методом прямой спектрофотометрии с использованием ГСО пиностробина, также как и для сырья прополиса и почек тополя в качестве аналитической была выбрана длина волны 289 нм, соответствующая максимуму поглощения ГСО пиностробина [1–4, 6]. Методика количественного определения суммы БАС в лекарственном средстве «Прополиса настойка» унифицирована с сырьем прополиса [1–4, 6] и выглядит следующим образом: 1,00 мл препарата помещают в мерную колбу вместимостью 50 мл, доводят объем раствора до метки 96 % спиртом и перемешивают (раствор А). 1 мл раствора А помещают в мерную колбу вместимостью 50 мл, доводят объем раствора до метки 96 % спиртом и перемешивают (раствор Б). Измеряют оптическую плотность раствора Б на спектрофотометре при длине волны 289 нм в кювете с толщиной слоя 10 мм. Параллельно в тех же условиях измеряют оптическую плотность раствора Б ГСО пиностробина. В качестве раствора сравнения используют 96 % этиловый спирт. Содержание суммы флавоноидов и фенилпропаноидов в препарате в процентах (Х) в пересчете на пиностробин вычисляют по формуле:
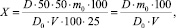
где D – оптическая плотность испытуемого раствора (раствор Б); D0 – оптическая плотность раствора Б ГСО пиностробина; m0 – масса ГСО пиностробина, г; V – объем испытуемого препарата, мл.
Приготовление раствора ГСО пиностробина. Около 0,02 г (точная навеска) ГСО пиностробина (ФС 42-0073-00) растворяют в мерной колбе вместимостью 100 мл в 80 мл 96 % спирта при нагревании (70–75 °С). Содержимое колбы охлаждают и доводят объем раствора тем же спиртом до метки и перемешивают (раствор А). 1 мл полученного раствора А помещают в мерную колбу вместимостью 25 мл и доводят объем раствора до метки 96 % спиртом этиловым (раствор Б).
Результаты статистической обработки проведенных опытов свидетельствуют о том, что относительная ошибка отдельного определения с доверительной вероятностью 95 % составляет 4,44 % (табл. 2).
Таблица 2
Метрологические характеристики методики определения суммы флавоноидов и фенилпропаноидов в препарате «Прополиса настойка»
|
f |
x, % |
s |
P, % |
t (P, f) |
Dx |
e, % |
|
10 |
1,655 |
0,033 |
95 |
2,23 |
± 0,074 |
± 4,44 |
f – число степеней свободы;
x – среднее выборки;
s – стандартное отклонение;
Р – доверительная вероятность;
t(P, f) – значение критерия Стьюдента;
Dx – полуширина доверительного интервала;
ε – относительная ошибка отдельного определения.
Опыты с добавками ГСО пиностробина к препарату показали, что ошибка опыта находится в пределах ошибки единичного определения, что свидетельствует об отсутствии систематической ошибки разработанной методики (табл. 3).
Таблица 3
Результаты опытов с добавками ГСО пиностробина
|
№ п/п |
Содержание действующих веществ в 1 мл препарата (мг) |
Добавлено ГСО пиностробина (мг) |
Найдено (мг) |
Ошибка |
|
|
Абсолютная (мг) |
Относительная (%) |
||||
|
1 |
16,4 ± 0,7 |
11,1 |
27,1 ± 1,2 |
–0,4 |
–1,46 |
|
2 |
16,4 ± 0,7 |
22,2 |
37,1 ± 1,7 |
–1,5 |
–3,89 |
|
3 |
16,7 ± 0,7 |
11,1 |
28,7 ± 1,3 |
+0,9 |
+3,24 |
|
4 |
16,7 ± 0,7 |
22,2 |
40,2 ± 1,8 |
+1,3 |
+3,34 |
Разработанная методика количественного определения суммы флавоноидов и фенилпропаноидов в препарате включена в проект ФС «Прополиса настойка».
Проведено количественное определение содержания суммы флавоноидов и фенилпропаноидов в препарате «Прополиса настойка» в пересчете на ГСО пиностробина, оно составило от 1,4 до 2,1 % (табл. 1). Данный показатель рекомендован для включения в проект ФС на лекарственное средство «Прополиса настойка» – не менее 1,0 %.
Выводы
1. Разработаны унифицированные с сырьем новые методики определения подлинности прополиса настойки, заключающиеся в использовании прямой и дифференциальной спектроскопии после добавки треххлорного алюминия.
2. Разработана унифицированная методика количественного спектрофотометрического определения содержания суммы флавоноидов и фенилпропаноидов в прополиса настойке с использованием ГСО пиностробина, которая рекомендована для включения в проект ФС «Прополиса настойка» взамен ФС 42-3736-99. Результаты статистической обработки проведенных определений свидетельствуют о том, что относительная ошибка отдельного определения с доверительной вероятностью 95 % составляет 4,44 %.
3. При помощи разработанной методики определено количественное содержание суммы флавоноидов и фенилпропаноидов в заводских серийных образцах «Прополиса настойка», которое колебалось от 1,4 до 2,1 %. Для ФС рекомендуется нижний предел данного показателя – не менее 1,0 %.
Рецензенты:
Куркин В.А., д.фарм.н., профессор, заведующий кафедрой фармакогнозии с ботаникой и основами фитотерапии, ГБОУ ВПО СамГМУ Минздрава России, г. Самара;
Первушкин С.В., д.фарм.н., профессор, заведующий кафедрой фармацевтической технологии, ГБОУ ВПО «Самарский государственный медицинский университет» Министерства здравоохранения РФ, г. Самара.
Работа поступила в редакцию 01.08.2013.



