Среди описанных в литературе 2-гетарилтиено[2,3-b]пиридин-3-иламинов нами не найдено ни одного примера 2-(2-тиенил) производных. В то же время синтез, стереохимия, превращения и биологические свойства их ближайших аналогов – 2-(2-фурил) производных хорошо изучены [2, 6]. Целью настоящей работы является синтез 2-(2-тиенил)тиено[2,3-b]пиридин-3-иламинов, изучение их превращений и стереохимии синтезированных веществ, используя возможности квантово-химического моделирования с применением теории функционала плотности [5, 7] в программном комплексе HyperChem 8.03.
Для синтеза искомых веществ использована реакция 2-меркаптоникотинонитрилов 1а,б с метил 5-(бромметил)тиофен-2-карбоксилатом 2 в присутствии биэквивалентного количества КОН, протекающая в два этапа (алкилирование и последующая гетероциклизация по Торпу-Циглеру). При этом метил 5-(3-аминотиено[2,3-b]пиридин-2-ил)-2-тиофенкарбоксилаты 3 получены с выходом более 85 % (табл. 1).
Промежуточные продукты алкилирования 4а,б также выделены в свободном виде, охарактеризованы и введены в реакцию с эквивалентным количеством КОН. Выход продуктов 3а,б в пересчете на исходные никотинонитрилы примерно такой же, как в первом случае. Однако в первом случае при проведении «оnе-роt»-процесса экономится растворитель и сокращается время синтеза.
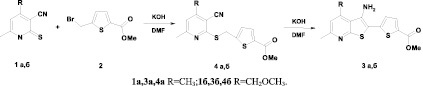
Схема 1
Таблица 1
Данные элементного анализа, температуры плавления и выходы соединений 3–7
|
Соединение |
Брутто-формула |
Найдено, % Вычислено, % |
Тпл, °С |
Выход, % |
||
|
C |
H |
N |
||||
|
3а |
C15H14N2O2S2 |
56,46 56,58 |
4,44 4,43 |
8,76 8,80 |
204–205 |
85 |
|
3б |
C16H16N2O3S2 |
54,98 55,15 |
4,61 4,63 |
8,03 8,04 |
164–165 |
87 |
|
4а |
C15H14N2O2S2 |
56,49 56,58 |
4,47 4,43 |
8,85 8,80 |
153–154 |
83 |
|
4б |
C16H16N2O3S2 |
55,05 55,15 |
4,59 4,63 |
8,12 8,04 |
126–128 |
85 |
|
5 |
C23H20N2O4S2 |
59,98 61,04 |
4,43 4,45 |
6,19 6,19 |
99–100 |
96 |
|
6 |
C20H18N2O3S2 |
59,88 60,28 |
4,49 4,55 |
7,00 7,03 |
201–202 |
75 |
|
7 |
C15H16N4O2S2 |
51,66 51,70 |
4,60 4,63 |
15,99 16,08 |
220–221 |
80 |
Данные элементного анализа, температуры плавления и выходы соединений 3 и 4 представлены в табл. 1. Метил 5-(3-аминотиено[2,3-b]пиридин-2-ил)-2-тиофенкарбоксилаты 3а,б – кристаллы желтого цвета, в то время как S-алкилпроизводные 4а,б – бесцветные вещества. Как следует из табл. 1, температуры плавления тиено[2,3-b]пиридинов 3 существенно выше, чем их нециклических изомеров 4.
В сравнении с ИК спектрами S-алкилпроизводных 4а,б в спектрах продуктов их изомеризации по Торпу-Циглеру 3а,б исчезает полоса валентных колебаний цианогруппы соответственно при 2218 и 2220 см–1, а также появляются две полосы валентных колебаний νN-H в области 3453–3412 и 3372–3319 см–1 (табл. 2). В спектрах ЯМР 1Н соединений 3а,б наблюдаются: исчезновение синглетных сигналов протонов при 4,77 и 4,54 м.д., соответствующих группе S-CH2 алкилпроизводных 4а,б; появление уширенных синглетов с интенсивностью 2Н, регистрирующихся при 5,35 и 5,74 м.д., соответствующих аминогруппе, в положении 3, что является характерным для тиено[2,3-b]пиридинов [4].
Исследование реакционной способности NH2-группы метил 5-(3-аминотиено[2,3-b]пиридин-2-ил)-2-тиофенкарбоксилатов с электрофильными реагентами проведено на примере соединения 3б, которое легко реагирует с хлористым бензоилом и диметокситетрагидрофураном (схема 2).
Моноацилирование 3б бензоилхлоридом проводится при кипячении в хлороформе при 10 % избытке хлорангидрида. N-Бензоилпроизводное 5 выделяется в виде бесцветных кристаллов с выходом 96 % (табл. 1).
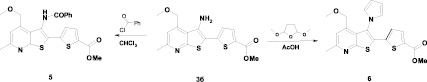
Схема 2
Реакцию 5-(3-аминотиено[2,3-b]пиридин-2-ил)-2-тиофенкарбоксилата 3б с 2,5-диметокситетрагидрофураном осуществляют аналогично [3] при кипячении в уксусной кислоте, используя 20 % избыток диметокситетрагидрофурана. Как и в случае ацилирования бензоилхлоридом, реакционная масса в процессе синтеза обесцвечивается. Образующееся 3-(1-пирролил) производное представляет собою бесцветное кристаллическое вещество, хорошо растворимое в полярных растворителях, его выход составляет 75 % (табл. 1).
5-(3-Амино-6-метил-4-метоксиметилтиено[2,3-b]пиридин-2-ил)-2-тиофенкарбогидразид 7 получают взаимодействием 3б с гидразингидратом в этаноле с выходом 80 %.
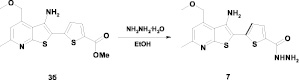
Схема 3
Таблица 2
Данные ИК и ЯМР 1Н спектров исследуемых соединений 3–7
|
Соединение |
ИК спектр, ν, см–1 |
Спектр ЯМР 1Н (δ, м. д. и КССВ, J, Гц) |
|
3а |
3453,3372 (NH); 1701 (С = Осл.эфира); 1298 (С–О–Ссл.эфира) |
2,50, 2,77 (оба с, по 3Н, 4-СН3Py, 6-CH3Py ); 3,83 (с, 3Н, COOСН3); 5,35 (уш. с, 2Н, NH2); 7,03 (с, 1Н, 5-НPy); 7,30 (д, 1Н, 4-Нтиофена, J = 4,1); 7,79 (д, 1Н, 3-Нтиофена, J = 4,1) |
|
3б |
3412,3319 (NH); 1711 (C = Oсл. эфира); 1279 (С–О–С) |
2,55 (с, 3Н, 6-CH3); 3,38 (с, 3Н, ОСН3); 3,83 (с, 3Н, COOСН3); 4,84 (с, 2Н, ОСН2); 5,74 (уш. с, 2Н, NH2); 7,24 (с, 1Н, 5-НPy); 7,31(д, 1Н, 4-Нтиофена, J = 4,1); 7,79 (д, 1Н, 3-Нтиофена, J = 4,1) |
|
4а |
2218 (СN); 1701 (С = Осл.эфира); 1298 (С–О–Ссл.эфира) |
2,41, 2,56 (оба с, по 3Н, 4-СН3Py, 6-CH3Py); 3,77 (с, 3Н, СOOCН3); 4,77 (с, 2Н, SСН2); 7,16, (д, 1Н, 4-Нтиофена, J = 3,7); 7,18 (с,1Н, 5-HPy), 7,61 (д, 1Н, 3-Нтиофена, J = 3,7) |
|
4б |
2220 (СN); 1715 (С = Осл.эфира); 1279 (С–О–Ссл.эфира) |
2,61 (с, 3Н, 6-CH3 Py); 3,37(с, 3Н, 4-ОСН3); 3,77 (с, 3Н, COOСН3); 4,54 (с, 2Н, SСН2), 4,79 (с, 2Н, ОСН2); 7,20, (д, 1Н, 4-Нтиофена, J = 3,7); 7,26 (с,1Н, 5-HPy); 7,61 (д, 1Н, 3-Нтиофена, J = 3,7) |
|
5 |
3482 (NH); 1709 (С = Осл. эфира); 1659 (С = Оамида); 1279 (С–О–Ссл.эфира) |
2,55 (с, 3Н, 6-CH3Py) ; 2,87 (с, 3Н, 4-ОСН3); 2,95 (с, 3Н, СООСН3), 3,72 (с, 2Н, ОСН2); 6,55 (с, 1Н, НPy; 6,75 (д, 1Н, 4-Нтиофена, J = 4,1), 6,81(дд, 2Н, 3,5-НPh,J = 6,8,J = 6,3); 6,87 (д, 1Н, 4-НPh, J = 6,3), 6,97 (д, 1Н, 3-Нтиофена, J = 4,1); 7,24 (д, 2Н, 2,6-НPh, J = 6,8); 9,62 (с, 1Н, NH) |
|
6 |
1718 (C = Oсл. эфира); 1260 (С-О-С сл.эфира) |
2,60 (с, 3Н, 6-CH3 Py); 3,16 (с, 3Н, ОСН3), 3,78 (с, 3Н, COOСН3); 3,90 (с, 2Н, ОСН2), 6,47 (с, 2Н, β-НPyrrol); 6,95 (д, 1Н, α-НPyrrol); 7,26( д, 1Н, 3-Нтиофена, J = 4,1); 7,36(с,1Н, 5-HPy), 7,70( д, 1Н, 3-Нтиофена, J = 4,1) |
|
7 |
1674 (С = Оамида); 3374, 3328 (NH); 3249, 3243, 3237 (NH) |
2,55 (с, 3Н, 6-СН3Py,); 3,38 (с, 3Н, ОСН3), 4,01 (с, 2Н, ОСН2); 6,41 (с, 1Н, НPy), 4,45 (уш. c, 2H, NNH2); 5,59 (уш.с, 2Н, NH2), 6,45 ( д, 1Н, 4-Нтиофена, J = 4,1) и 6,91 (д, 1Н, 3-Нтиофена, J = 4,1); 9,78 (с, 1Н, NH) |
Синтезированные тиофензамещенные тиенопиридины имеют систему сопряженных связей, что дает возможность предположить плоское или близкое к плоскому строение их молекул.
Для расчета геометрии исследуемых соединений 3а-7 использовался гибридный метод B3LYP [5,7]с обменным функционалом Беке (B3) и корреляционным функционалом Ли-Янга–Парра (LYP) в валентно-расщепленном базисном наборе 6–31G(d,p) с добавлением шести поляризационных d-функций для неводородных атомов и трех p-функций для атомов водорода. Результаты расчета торсионных углов, длин связей приведены в табл. 3.
Как показывают данные торсионных углов S–C–C–S, тиенопиридиновый и тиофеновый фрагменты незначительно отклоняются от копланарности. На это же указывают укороченные длины связи С–С между тиенопиридиновым и тиофеновым циклами, составляющие 1,44–1,45 Å, что является следствием сопряжения между этими фрагментами. Атомы серы тиофенового и тиенопиридинового фрагментов соединений 3а, 3б, 5, 7 направлены в противоположные стороны, что обусловлено выгодностью конформации, в которой осуществляется перекрывание ароматических π-систем указанных выше фрагментов.
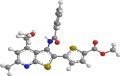
В случае же соединения 6 торсионный угол S–C–C–S составляет 20°, что можно объяснить электронным отталкиванием атома серы тиофенового кольца от π-системы пиррольного кольца, расположенного почти перпендикулярно плоскости тиенопиридина (торсионный угол С–С-N–С равен 77°). На отсутствие сопряжения пиррольного и тиенопиридинового фрагмента указывает длина связи C–N, равная 1,42 Å (наибольшая из рассматриваемых соединений). Именно поэтому атомы серы тиофенового и тиенопиридинового фрагментов направлены в одну сторону (рисунок).
Таблица 3
Данные расчета торсионных углов и длин связей соединений 3, 5, 6, 7
|
Параметры |
Соединения |
||||
|
3а |
3б |
5 |
6 |
7 |
|
|
Торсионный угол SCCS, ° |
156,9 |
159,7 |
150,7 |
19,9 |
156,3 |
|
Торсионный угол SCCO, ° |
0,5 |
0,8 |
0,9 |
0 |
168,2 |
|
Торсионный угол ССNC, ° |
– |
– |
114,8 |
76,6 |
– |
|
Длина водородной связи О⋅Н, Å |
– |
1,92 |
1,94 |
– |
1,92 |
|
Валентный угол водородной связи О⋅Н–N, ° |
– |
152,7 |
144,9 |
– |
152,6 |
|
Длина связи SC-CS, Å |
1,44 |
1,44 |
1,45 |
1,45 |
1,44 |
|
Длина связи SC–CO, Å |
1,46 |
1,46 |
1,47 |
1,47 |
1,48 |
|
Длина связи C–N, Å |
1,39 |
1,38 |
1,41 |
1,42 |
1,39 |
3а 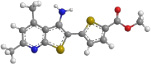 3б
3б 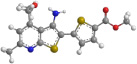
 6
6 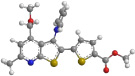 7
7 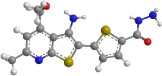
Модели молекул синтезированных соединений 3а, 3б, 5, 6, 7
Для соединений 3б, 5 и 7 возможно предположить образование водородной связи между атомами водорода аминогруппы и кислорода метоксиметильного заместителя, поскольку расстояние между этими атомами не превышает 1,95 Å (табл. 3). Этот факт подтверждается данными РСА для фуротиено[2,3-b]пиридина схожего строения, где валентный угол O·H–N в семичленном экзоцикле составляет 145–153°[1]. Как показывает расчет (табл. 3), сопряжение наблюдается между тиофеновым и сложноэфирным (соединения 3а, 3б, 5, 6), а также тиофеновым и гидразидным (соединение 7) фрагментами. Длина связи SC-CO составляет 1,46–1,48 Å.
Карбонильная группа сложноэфирного фрагмента для соединений 3а, 3б, 5, 6 расположена копланарно с тиофеновым циклом и направлена в одну сторону с атомом серы. Для соединения 7 копланарность тиофенового и сложноэфирного фрагментов не нарушается, но атом серы и карбонильный кислород имеют противоположные направления, что может быть связано с более эффективным перекрыванием орбитали атома азота гидразинового фрагмента с π-орбиталями углеродных атомов тиофенового кольца, которое приводит к более энергетически выгодной транс-конфигурации фрагмента S-C-C-O.
Данные квантово-химических расчетов показывают, что все связи в соединениях 3, 5, 6, 7 (исключение составляет связь С-N в соединении 6) укорочены, т.е. являются сопряженными. Поэтому представлялось интересным проследить передачу электронных эффектов в исследуемых молекулах. Так в ИК-спектре соединения 6 валентные колебания карбонильной группы находятся в более высокочастотной области спектра 1718 см–1, что подтверждает её меньшее сопряжение с π-электронной системой молекулы, вследствие выхода пиррольного кольца из системы сопряжения и отсутствия его положительного мезомерного эффекта.
Проследить передачу электронных эффектов в молекулах методом ЯМР 1Н весьма затруднительно, так как заместители, имея π-системы, являются анизотропными. Однако, как показывают данные табл. 2, замена метильной группы в положении 4 тиенопиридинового фрагмента (соединение 3а) на метоксиметильную (соединение 3б), обладающую отрицательным индукционным эффектом, приводит к слабопольному сдвигу протона 5-НPy – на 0,22 м.д. и протонов аминогруппы на 0,39 м.д.
Сигналы протонов соединения 7 аминогруппы прописываются в более сильном поле, чем для исходного соединения 3б, что вызвано заменой сложноэфирной группы соединения 3б на гидразидную. Для соединения 6 закономерным являются слабопольный сдвиг протона 5-НPy на 0,12 м.д. в связи с проявлениями отрицательного индукционного эффекта атома азота пиррольного кольца и отсутствием положительного мезомерного эффекта последнего вследствие особенностей стереоструктуры молекулы, обсужденной выше. Протоны CH2О группировки соединения 6, наоборот, имеют сильнопольное смещение на 0,94 м.д., что вызвано анизотропным влиянием пиррольного кольца.
Экспериментальная часть
Спектры ЯМР 1Н зарегистрированы на спектрометре BrukerDRX-500 (500,13 МГц, внутренний стандарт ТМС) в ДМСО-d6. ИК спектры записаны на приборе ИнфраЛЮМ ФТ-02 (суспензия в вазелиновом масле). Элементный анализ выполнен на C,H,N анализаторе Carlo-Erba (модель 1106). Чистоту полученных соединений контролировали методом ТСХ на пластинах SilufolUV-254, элюент толуол-этанол, 3:1 или ацетон-гексан, 1:1; детектирование УФ-светом или парами йода.
Метил 5-(3-амино-4,6-диметилтиено[2,3-b]пиридин-2-ил)-2-тиофенкарбоксилат3а
Смешивают взвесь 5 ммоль 2-меркапто-4,6-диметилникотинонитрила 1а в 10 мл ДМФА и 2,8 мл 10 % водного раствора гидроксида калия. После гомогенизации смеси добавляют 5 ммоль 5-бромометилтиофенкарбоксилата. Реакционную смесь перемешивают 1 час при температуре 65–70 °С. Далее в реакционную смесь добавляют ещё 2,8 мл 10 % водного раствора КОН, после чего раствор кипятят в течение 3 часов. Кристаллы продукта отделяют, промывают водой, сушат и перекристаллизовывают из смеси C2H5OH-ДМФА. Выход – 85 %.
Соединение 3б получают аналогично. Выход 87 %.
Метил 5-(4,6-диметил -3-циано-2-пиридилсульфанилметил)-2-тиофенкарбоксилат4а
Смешивают взвесь 5 ммоль 2-меркапто-4,6-диметилникотинонитрила 1а в 10 мл ДМФАи 2,8 мл 10 % водного раствора гидроксида калия. После гомогенизации смеси добавляют 5 ммоль 5-бромометилтиофенкарбоксилата. Реакционную смесь перемешивают 1 час при температуре 65–70 °С, затем охлаждают и разбавляют 15 мл воды. Кристаллы продукта отделяют, промывают водой, сушат и перекристаллизовывают из смеси C2H5OH-ДМФА. Выход – 83 %.
Соединение 4б получают аналогично. Выход – 85 %.
Метил 5-(6-метил-4-метоксиметил-3-фенилкарбоксамидотиено[2,3-b]пиридин-2-ил)-2-тиофенкарбоксилат5
К раствору 10 ммольметил 5-(3-амино-6-метил-4-метоксиметилтиено[2,3-b]пиридин-2-ил) -2-тиофенкарбоксилата (3б) в 20 мл хлороформа прибавляют 11 ммоль бензоилхлорида. Реакционную смесь кипятят в течение 1,5 ч. Растворитель упаривают почти полностью. Остаток обрабатывают 10 % водным раствором аммиака. Кристаллы продукта отделяют, промывают водой, сушат на воздухе и перекристаллизовывают из ДМФА. Выход – 96 %.
Метил 5-[6-метил-4-метоксиметил-3-(1Н-1-пирролил)тиено[2,3-b]пиридин-2-ил]-2-тиофенкарбоксилат6
Раствор 3 ммоль метил 5-(3-амино-6-метил-4-метоксиметилтиено[2,3-b]пиридин-2-ил) -2-тиофенкарбоксилата (3б) в 4 мл ледяной уксусной кислоты нагревают до кипения и вносят при перемешивании 3,6 ммоль 2,5-диметокситетрагидрофурана. Реакционную массу кипятят в течение 40 минут, охлаждают и разбавляют 20 мл воды. Образовавшийся осадок отделяют, промывают водой до нейтральной реакции промывных вод, сушат и перекристаллизовывают из этанола. Выход – 75 %.
5-(3-амино-6-метил-4-метоксиметилтиено[2,3-b]пиридин-2-ил)-2-тиофенкарбогидразид7
К суспензии 3 ммоль метил 5-(3-амино-6-метил-4-метоксиметилтиено[2,3-b]пиридин-2-ил)-2-тиофенкарбоксилата (3б) в 20 мл этанола, прибавляют 15 ммоль гидразина в виде 24 % водного раствора. Реакционную смесь кипетят в течение 4,5 ч. Далее реакционную массу упаривают втрое. Кристаллы соединения 7 отфильтровывают, промывают водой и спиртом, сушат и перекристаллизовывают из ДМФА. Выход – 80 %.
Рецензенты:
Посконин В.В., д.х.н., профессор, кафедра химии, сертификации и метрологии КубГТУ, г. Краснодар;
Стрелков В.Д., д.х.н., профессор, заведующий лабораторией регуляторов роста растений ГНУ ВНИИБЗР, г. Краснодар.
Работа поступила в редакцию 08.11.2013.



