Термический ожог органов дыхания является тяжёлой травмой и часто приводит к летальному исходу. Термический ожог сопровождается мощным окислительным стрессом, развитием воспалительного процесса, интенсивным некрозом и апоптозом клеток респираторного эпителия [4]. Эффективное лечение термических ожогов дыхательных путей подразумевает нейтрализацию всех этих последствий
В случае верхних дыхательных путей антиоксидантная система представлена набором ферментов-антиоксидантов, основным из которых является пероксиредоксин 6 (Prx6). Согласно литературным данным, паракринные факторы мезенхимальных стволовых клеток (МСК) обладают прогенераторным, антивоспалительным и антиапоптотическим действием [6]. Таким образом, использование экзогенного Prx6 нейтрализует окислительный стресс, а паракринные факторы должны способствовать ускорению восстановления поврежденной ткани.
Задача – оценить терапевтический эффект пероксиредоксина 6, паракринных факторов мезенхимальных стволовых клеток и смеси этих препаратов при эндотрахеальной инсталляции после термического ожога, сравнить интенсивность регенерации эпителия в этих трёх случаях и сделать вывод о наиболее эффективном из них.
Материалы и методы исследования
В экспериментах использовали крыс линии «Вистар» мужского пола весом 250 г.
Термический ожог и эндотрахеальная инсталляция препаратов.
Используемый в работе рекомбинантный человеческий пероксиредоксин 6 был получен в лаборатории механизмов рецепции Института биофизики клетки РАН. Данный фермент-антиоксидант имеет удельную пероксидазную активность по Н2О2 120 мкм/мг/мин и по трет-бутил гидропероксиду 80 мкм/мг/мин [5].
Белки из культуральной среды мезенхимальных стволовых клеток свиньи были получены в НИИ им. Склифосовского. Эти белки представляют собой набор паракринных факторов культивируемых стволовых клеток, среди них обнаружены различные факторы роста, а также большое количество интерлейкина 6.
Термический ожог верхних дыхательных путей крысы проводили посредством микропарогенератора с аппликацией горячего пара температурой 70° непосредственно в трахею крысы в течение 4–8 секунд. Ранее было показано, что ожог в течение этого времени вызывает значительное повреждение эпителия трахеи [2]. Предварительно животное наркотизировалось путём внутрибрюшинного введения препаратов «Золетил» (2 мг препарата/100 г массы животного) и «Рометар» (25 мкл каждому животному).
Растворы белков были введены эндотрахеально через 10 минут после нанесения ожоговой травмы. Объём вводимого раствора во всех случаях – 200 мкл. Концентрация Prx6 и концентрация белков среды МСК в равна 1 мг/мл. Количество апплицированного белка составило 200 мкг каждому животному.
Гистологический анализ
Для проведения гистологических исследований эпителиальной ткани трахеи выделенные образцы фиксировали в фиксаторе «Mirsky’s Fixative» (National Diagnostics, USA) в течение 48 часов. После этого ткань проводили через растворы спирта восходящей концентрации и заключали в парафин. Срезы толщиной 2–3 мкм получали на микротоме Thermo scientific micron HM 325, Германия. Для окрашивания срезов был использован эозин-гематоксилин (Fluka, Швеция).
Результаты исследования и их обсуждение
В эксперименте участвовало четыре группы крыс. Все животные получили термический ожог одинаковой силы, трём из четырёх групп после ожога были введены препараты. Первой группе – раствор белков среды МСК, второй группе – раствор пероксиредоксина 6, третьей – смесь этих растворов. Отбор образцов трахеи был проведён через 1 сутки, 3 суток и 7 суток после ожога.
Морфология эпителия трахеи крыс первой группы (без введения препарата) и морфология здоровой трахеи (контроль) представлены на рис. 1.
1 2
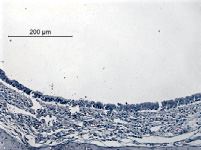
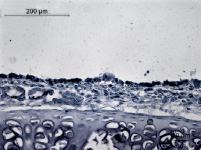
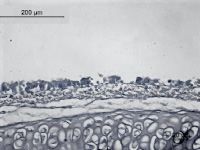
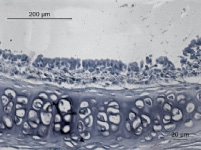
Рис. 1. Морфология эпителия трахеи крысы без ожога – 1а; морфология эпителия трахеи через сутки после ожога – 2а; морфология эпителия трахеи через 3 суток после ожога – 1б; морфология эпителия трахеи через 7 суток после ожога – 2б
На рис. 1а представлен неповреждённый эпителий трахеи. Видны основные типы клеток респираторного эпителия: реснитчатые, бокаловидные и базальные. Различимы реснички, присущие реснитчатым клеткам респираторного эпителия. При ожоге наблюдается массовая гибель всех типов клеток, сопровождаемая истончением эпителия (рис. 1б). На третьи сутки начинается заметное восстановление, на седьмой день эпителий выглядит частично восстановленным (рис. 1б, 2б).
Рис. 2 иллюстрирует морфологию респираторного эпителия после термического ожога и последующей аппликации в трахею препаратов. В случае использования паракринных факторов МСК мы видим, что массовая гибель клеток не была предотвращена (рис. 1а). В то же время регенерационные процессы в эпителии усилены, что показано на рис. 1б и в. Аппликация фермента-антиоксиданта пероксиредоксин 6 в трахею после ожога существенно уменьшает гибель клеток сразу после ожога, и эпителий остаётся частично сохранённым (рис. 2а). Аппликация в трахею после ожога одновременно Prx6 и паракринных факторов МСК практически полностью сохраняет респираторный эпителий (рис. 3а).
Как свидетельствуют полученные результаты, термический ожог верхних дыхательных путей вызывает сильное разрушение эпителия трахеи в первые же часы после ожога. Темп естественного восстановления трахеи позволяет заметить улучшения спустя семь суток после ожога. Применение паракринных факторов МСК, в отличие от применения Prx6, не оказывает значительного влияния на сохранение эпителия сразу после ожога. Таким образом, нейтрализация окислительного стресса действительно является необходимым условием сохранения эпителия, по крайней мере при ожоговой травме.
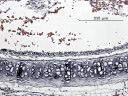



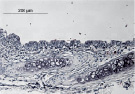



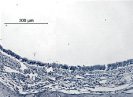
Рис. 2. Морфология трахеи крысы после термического ожога и эндотрахеальной инсталляции раствора белков среды МСК и Prx6: аппликация паракринных факторов МСК – 1а (через сутки), 1б (через трое суток), 1в (через семь суток); аппликация Prx6 – 2а (через сутки), 2б (через трое суток), 2в (через семь суток); аппликация смеси этих препаратов – 3а (через сутки), 3б (через трое суток), 3в (через семь суток)
В то же время применение паракринных факторов МСК значительно ускоряет регенерацию эпителиальной ткани, приблизительно в два раза по сравнению с контролем.
Следовательно, оптимальными условиями восстановления эпителия трахеи после термического ожога являются:
1) нейтрализация окислительного стресса;
2) интенсификация процессов регенерации в эпителиальной ткани.
В данной работе первое условие выполняется путём применения антиоксидантов [1, 3, 4, 7], второе – с помощью факторов роста, которые в большом количестве содержатся в среде МСК. Как следствие, наилучший терапевтический результат имеет место в ситуации совместного действия препаратов, то есть наблюдается синергизм действия фермента-антиоксиданта Prx6 и паракринных факторов МСК при лечении термической ожоговой травмы органов дыхания.
При совместном использовании белков среды МСК и Prx6 в подслизистом слое трахеи были замечены замкнутые структуры, морфологически подобные эпителию (рис. 2, 3а–в). Их количество достигает максимума к третьему дню после ожога, затем идёт на убыль, и к седьмому дню подслизистый слой возвращается к нормальному виду. Примечательно, что данные структуры наблюдаются только при совместном использовании фермента-антиоксиданта и паракринных факторов, в случае же их раздельной аппликации в трахею, а также в случае отсутствия лечения после ожога и в норме эти структуры встречаются крайне редко.
Заключение
Исследовали терапевтический эффект, который оказывают на респираторный эпителий трахеи крысы после термического ожога пероксиредоксин 6 и белки среды МСК вместе и по отдельности. Сделали вывод об оптимальности совместного использования этих препаратов. Это объясняется необходимостью одновременного устранения окислительного стресса и активации роста новых клеток для достижения наибольшего эффекта в лечении ожоговых травм.
Полученные результаты могут быть использованы в создании лекарственных препаратов, предназначенных для лечения ожоговых травм верхних дыхательных путей [3].
Работа поддержана грантом РФФИ 13-04-00537 и грантом Президиума РАН «Молекулярная и клеточная биология».
Рецензенты:Куликов А.В., д.б.н., заведующий лабораторией клеточно-тканевых механизмов компенсации функций биообъектов, ФГБУН «Институт теоретической и экспериментальной биофизики» РАН, г. Пущино;
Новосёлова Е.Г., д.б.н., главный научный сотрудник, ФГБУН «Институт биофизики клетки» РАН, г. Пущино.
Работа поступила в редакцию 05.02.2015.



