Поиск новых способов повышения эффективности приживаемости костных имплантов является одной важнейших задач в ортопедии, хирургии и стоматологии [2,4]. Наиболее перспективным направлением в остеосинтезе является использование наноматериалов [1,6]. Благодаря своим особым свойствам наноматериалы и нанокомпозиты, включающие наночастицы, обладают большей прочностью, гибкостью, химической устойчивостью. Основным камнем преткновения в развитии этого направления является недостаточно отработанный механизм оценки безопасности и эффективности использования нанокомпозитов. Для использования наноматериалов требуются уникальные оценки риска, учитывая новизну и разнообразие продуктов, высокую подвижность и реакционную способность проектируемых наночастиц [3,5]. Исследования коллаген-гидроксиапатитной матрицы, имитирующей структуру и химические свойства природной костной ткани, являются уникальными не только в российском, но и международном масштабе. В Государственном учреждении Научно-исследова-тельский институт эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи Российской академии медицинских наук были разработаны экспериментальные модели нанокомпозитов, состоящие из наноколлагена и наногидроксиапатита. Целью нашего исследования являлось изучение на различных структурных уровнях морфофункциональных особенностей регенерации костной ткани при внедрении нанокомпозитов.
Материалы и методы
Эксперимент выполняли на 40 крысах-самцах линии "Вистар" массой 200-250 г, которые были разделены на 4 группы:
1 группа - оперативное внедрение смеси коллаген 2,0 г/л, ГАП 18%, экспозиция 7 дней;
2 группа - оперативное внедрение смеси коллаген 2,0 г/л, ГАП 18%, экспозиция 21 день;
3 группа - оперированные животные без введения композита, экспозиция 7 дней;
4 группа - оперированные животные без введения композита, экспозиция 21 день.
В условиях общего обезболивания ингаляцией паров эфира после выстригания волосяного покрова и туалета операционного поля раствором йодоната производился разрез мягких тканей черепа до кости. Теменная область скелетировалась распатором на площади, необходимой для размещения импланта. В связи с тонкостью кости трифинация черепа производилась брюшистым скальпелем. Из образованного отверстия микрокусачками выполнялась частичная резекция кости с образованием дефекта свода черепа. Гемостаз осуществляли тампонадой стерильными салфетками, смоченными 3%-ным раствором перекиси водорода. В условиях «сухой» раны на костный дефект располагался композит без жесткой фиксации. Рана ушивалась наглухо. Туалет раны осуществлялся раствором бриллиантового зеленого без наложения защитной повязки. Профилактика гнойных осложнений осуществлялась соблюдением правил асептики и антисептики. Животных выводили из опыта через 7 и 21 суток посредством передозировки эфирного наркоза. На аутопсии для гистологического исследования из черепа вырезались прооперированные участки 0,5х0,5 см3, которые затем фиксировали в 10%-ном нейтральном формалине.
Для световой микроскопии тканевые образцы заключали в парафин, затем на микротоме готовили срезы с последующей окраской их гематоксилином и эозином и подвергали исследованию в микроскопе «TOPIC-T» CETI. Для сканирующей электронной микроскопии пробы помещали в фиксирующую смесь: 2% глутаральдегид на 0,15 М фосфатном буфере с pH 7,2-7,4, а затем просматривали в растровом микроскопе FE1 Quanta 200 3D.
Результаты исследования
Все прооперированные животные сохранили жизнеспособность до конца исследования. В группах с введением нанокомпозитов уже через четыре часа были восстановлены двигательная активность и пищевое поведение. За время проведения эксперимента животные не болели, внешний вид, за исключением шва в теменной области, соответствовал неоперированным особям. Несколько отличалось поведение оперированных животных без введения нанокомпозита. Двигательная активность и пищевое поведение были восстановлены только через 12 часов, однако еще в течение 7 суток оно значительно отличалось от поведения животных, у которых дефект был заполнен нанокомпозитом. По истечении 21 суток поведение всех животных было полностью стандартным.
При изучении прооперированных участков в группах с введением нанокомпозитов с 7-дневной экспозицией нами была получена следующая картина. Макроскопически отмечено срастание краев кожного лоскута путем первичного натяжения. Отечность тканей практически отсутствует. Полнокровие умеренно выраженное. Достаточно четко выражена зона демаркационного воспаления. Оперированный участок светло-коричневого цвета. Микроскопически было показано начало формирования четкой капсулы вокруг импланта. В жировой клетчатке отмечался умеренный отек, слабая инфильтрация нейтрофильными лейкоцитами и макрофагами. В их цитоплазме иногда видны мелкие гранулы фагоцитированного композита. В образце видны многочисленные фрагменты гидроксиапатита. Часть таких образований делится на еще более мелкие фрагменты либо подвергается распаду. Помимо этого в импланте видны фрагменты коллагеновых волокон. Имплант пронизан тяжами грануляционной ткани. Вокруг импланта тяжи имели относительно зрелый характер и формировали тонкую соединительно-тонкую капсулу. В тяжах, прорастающих в глубь импланта, ткань менее зрелая, она содержит большое количество макрофагов и единичных многоядерных гигантских клеток, окружающих фрагменты коллагена, и скопления гидроксиапатита и принимающая участие в их резорбции (рис. 1). Часто вокруг фрагментов коллагена образуется самостоятельная тонкая микрокапсула. В грануляционной ткани, прорастающей в имплант, кроме макрофагов видны новообразованные сосуды калибра капилляров и тяжи пролиферирующих фибробластов. Электронно-микроскопически выявлено, что появляются отдельные фибробласты. Внутри композита видны нити четко контурированного коллагена, расположенного внутри гидроксиапатита. Вокруг импланта появляются отдельные новообразованные капилляры, размножающиеся почкованием из предшествующих. Наблюдается начало образования сосудов внутри импланта. Фибробласты в большей степени выражены в области капсулы. Содержание эритроцитов невелико. Обнаруживаются отдельные нейтрофилы и макрофаги, окружающие фрагменты импланта. Снаружи имплант покрывается тонкой надкостницей.
К 21-му дню макроскопически снаружи уже виден шов, заросший путем первичного натяжения. При вскрытии кожного лоскута место оперативного дефекта, заполненного нанокомпозитами, почти не отличалось от окружающих участков, в остальных группах было малозаметным. Композит покрывала хорошо сформированная надкостница с собственными сосудами. Микроскопически отсутствует граница между имплантом и окружающей костной тканью, что рассматривается нами как остеоинтеграция. Гидроксиапатит практически полностью резорбирован макрофагами. В их цитоплазме иногда видны мелкие гранулы фагоцитированного композита. Композит почти полностью замещен грануляционной тканью и коллагеновыми волокнами и заселен фибробластами костной ткани. В периферических отделах наблюдались клетки росткового уровня костной системы: остеобласты, остеоциты, остеокласты. Начинается оссификация импланта по периферии. В импланте имеются новообразованные коллагеновые волокна, располагающиеся рыхло и беспорядочно с межклеточным матриксом (рис. 2). Вокруг и внутри импланта развитая сеть новообразованных сосудов. Электронно-микроскопически выявлены единичные, без четких контуров остатки гидроксиапатита. Коллагеновые волокна композита разволокненные, наполовину разрушенные макрофагами. Значительно отличаются от них появившиеся короткие тонкие нити новообразованного коллагена, который в большом количестве присутствует в композите. Композит покрыт хорошо развитой надкостницей. Внутри импланта появились отдельные новообразованные капилляры. Сосудистая сеть вокруг импланта полностью восстановлена. Фибробласты густо заселили периферические части композита и в небольшом количестве присутствуют в центральных частях.
При изучении материала, полученного при декапитации группы ложнооперированых животных по истечении 7 и 21 дня после проведенной операции, нами было показано, что морфологическая картина значительно отличалась от групп, где дефект костной ткани был заполнен нанокомпозитом.
 .
.
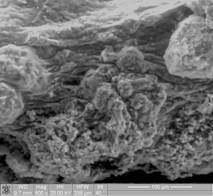
Рис. 1. Фрагмент костной ткани теменной части черепа с использованием нанокомпозита через 7 дней после имплантации.
В толще импланта новообразованная соединительная ткань
СЭМ. Ув. х 10000.
 .
.
Рис. 2. Фрагмент костной ткани теменной части черепа с использованием нанокомпозита через 21 день после имплантации.
В импланте имеются новообразованные коллагеновые волокна, располагающиеся рыхло и беспорядочно с межклеточным матриксом.
СЭМ. Ув. х 20000.
При изучении прооперированных участков в группе животных без введения композита с 7-дневной экспозицией нами была получена следующая картина. Макроскопически дефект и окружающие ткани были выражено гиперемированы. Сохранялся дефект костной ткани около 90%. Кожный лоскут, покрывающий дефект, был отечным. Микроскопически была выявлена выраженная лейкоцитарная и макрофагальная инфильтрация в костной ткани и окружающей клетчатке. Электронно-микроскопически были определены участки обширного гемолиза и некроза костной ткани.
Образцы с 21-дневной экспозицией напоминали аналогичное состояние у животных, прооперированных с введением композита через 7 дней. Так, макроскопически это проявлялось в сохранении костного дефекта, его покраснении и отечности окружающих тканей. Следует отметить, что дефект тканей превышал 30%, что было значительно больше, чем в предыдущих группах. Микроскопически нами показано, что в месте оперативного дефекта выявлялись проявления воспаления в виде полнокровия сосудов венозного русла в области предлежащей дермы и подкожной жировой клетчатки. Лейкоцитарная и макрофагальная реакции соответствовали картине образцов с заполнением дефекта нанокомпозитом с экспозицией 7 дней. Электронно-микроскопически выявлено, что наросшая на дефект надкостница была гистологически незрелой. Строение межклеточных контактов нарушено. Наблюдается увеличение просвета между клетками, что также усиливает диапедез и развитие экссудации. Наблюдается начало образования сосудов внутри надкостницы. Начинает формироваться фиброзная капсула. Фибробласты в большей степени выражены в области капсулы. Полость выстлана грануляционной тканью, в центре – новообразующиеся коллагеновые волокна и эритроциты. Последние в отдельных участках собираются в тромбы. Часть из эритроцитов гемолизирована.
Таким образом, регенерация костной ткани при заполнении дефекта нанокомпозитами идет значительно быстрее, чем без их применения, что доказывает отсутствие местного токсического влияния нанокомпозитов и их остеогенетические свойства. Сохранение нормальной двигательной активности и пищевого поведения указывает на отсутствие общего токсического влияния на организм лабораторных животных.
СПИСОК ЛИТЕРАТУРЫ
1. Васильев М.Г., Снетков А.И., Цуканов В.Е. и др. // Детская хирургия – 2006. – №2. – С. 44-48.
2. Григорьян А.С., Филонов М.Р., Топоркова А.К. // Архив патологии – 2008. – №3. – С. 36-37.
3. Снетков А.И., Лекишвили М.В., Касымов И.А. и др.// Вестн. травматол. и ортопед. – 2003. – № 4. – С. 103-122.
4. Павлова Т.В., Павлова Л.А., Павлов И.А. и др. // Систем. анализ и управл. в биомедицинск. системах. – 2007.– Т.6, № 2. – С. 364-366.
5. Павлова Т.В., Павлова Л.А., Павлов И.А., Кривецкий В.В. и др. // Международ. научно-практическая конференция «Достижения супрамолекулярной химии и биохимии в ветеринарии и зоотехники». – Москва, 2008. – С. 131-138.
6. Lemons J., Anabtawi M., Berk P., Morgan V. Histomorphometry of explanted dental implants. – New Orleans, 2007. – № 3.
Библиографическая ссылка
Т.В. Павлова, Ю.А. Мезенцев, Л.А. Павлова, А.В. Нестеров, Д.А. Колесников ОСОБЕННОСТИ РЕГЕНЕРАЦИИ КОСТНОЙ ТКАНИ ПРИ ВВЕДЕНИИ КОЛЛАГЕНОВО-ГИДРОКСИАПАТИТНЫХ НАНОКОМПОЗИТОВ // Фундаментальные исследования. – 2009. – № 8. – С. 25-28;URL: https://fundamental-research.ru/ru/article/view?id=1978 (дата обращения: 20.04.2024).



