Hейротрансмиттеры Ach и NE и пептидные гормоны холецистокинин, брадикинин и др. вызывают в клетках печени, поджелудочной железы, гладкомышечных клетках и адипоцитах белой жировой ткани регистрируются разнообразные типы сложных и простых Са2+-колебаний и автоволны, Са2+-спайки и триггерные переключения [2, 7–12]. Такое поведение характерно для клеток, выделенных из тканей и органов здоровых животных, хотя роль таких периодических и квазипериодических процессов в регуляции Са2+-сигнальных и метаболических систем до настоящего времени изучена недостаточно.
Известно, что ожирение и D2T приводят к существенным изменениям в экспрессии генов, контролирующих экспрессию белков – ферментов и каналов различных сигнальных и метаболических систем [3, 5]. Это в свою очередь может приводить к дисрегуляции различных сигнальных и метаболических систем и дисфункции соответствующих органов и тканей. При ожирении и Д2Т имеют место: инсулиновая резистентность, связанная с развитием стеатоза печени; стеатоз поджелудочной железы; гипертензия сосудов; гипертрофия и гибель адипоцитов и трансформация жировой ткани из активного буфера токсичных жирных кислот и важного эндокринного органа в орган, не способный запасать жирные кислоты и глюкозу, продуцирующий провоспалительные цитокины [1, 4, 6].
Поэтому изучение механизмов регуляции и закономерностей, приводящих к дисрегуляции Са2+-сигнальных и метаболических систем и к дисфункциии соответствующих органов и тканей при ожирении и D2T, является актуальным.
Материалы и методы исследования
В экспериментах использовали первичную культуру белых адипоцитов мыши на 9 день культивирования (9 DIV), полученную из мезенхимальной фракции стволовых клеток эпидидимального жирового депо и зрелые одиночные клетки без культивирования. Измерение динамики цитозольного кальция ([Ca2+]i) проводили с помощью системы анализа изображений «Cell observer» (Carl Zeiss, Германия), на базе моторизованного микроскопа Axiovert 200M с высокоскоростной черно-белой CCD-камерой AxioCam HSm. Источником света служила ртутная лампа НВО 100. Возбуждение флуоресценции Fura-2 проводили при двух длинах волн (340 и 387 нм) с использованием запирающих светофильтров BP 340/30 и BP 387/15.
Ожирение и D2T вызывали, скармливая животным свиной хребтовый жир в течение 10 месяцев с последующим отбором животных в группы: ожирения и D2T на основании измерений концентраций липидов, инсулина и глюкозы в крови. Критерии распределения животных на группы приведены в табл. 1.
Таблица 1
Здоровые животные, животные с ожирением и диабетом 2-го типа
|
Группы животных, состояние: |
Вес жировой ткани, (% веса) |
Глюкоза, (мМ) |
Инсулин, (нг/мл) |
Триглицериды, (мМ) |
Жирные кислоты, (мМ) |
Холестерин, (мМ) |
|
Здоровые |
< 15 |
4,0–6,0 |
< 0,5 |
0,5–1,2 |
0,3–1,2 |
1,5–2,5 |
|
Ожирение |
≥ 15 |
8,0–12,0 |
0,5–1,5 (2,0) |
1,0–2,0 |
1,5–2,5 |
2,5–4,5 |
|
Диабет 2-го типа |
> 15 |
12,0–20,0 |
2,0–3,5 |
1,8–2,5 |
1,5–3,0 |
4,0–6,0 |
Культивируемые адипоциты получали из преадипоцитов здоровых животных и из преадипоцитов животных с ожирением. Зрелые клетки выделяли из жировой ткани животных с D2T. Сравнительные эксперименты по экспрессии мРНК проводились с использованием образцов печени и жировой ткани животных с D2T (возраст – 1 год) и здоровых животных (возраст – 2–3 месяца).
Препараты тотальной РНК экстрагировали с помощью реагента Triazol (Sigma) и использовали в качестве матрицы при постановке реакции обратной транскрипции (ОТ) для получения кДНК. Перед постановкой реакции ОТ проводили определение концентрации тотальной РНК с помощью набора Quant-iTTM RNA BR Assay Kit на приборе QubitTM fluorometer (Invitrogen, USA). Реакцию ОТ проводили со случайными гексапраймерами (фирма «Синтол», Россия). Полученная кДНК использовалась для постановки полимеразной цепной реакции в режиме реального времени (RT PCR). Работа выполнена с использованием прибора 7300 Real-Time PCR System (Applied Biosystem, USA) Регионального Центра коллективного пользования УРАН ИТЭБ РАН. В качестве праймеров и зондов были использованы коммерчески доступные киты фирмы Applied Biosystem, (USA). Условия проведения реакции согласно рекомендациям фирмы производителя.
Результаты исследований и их обсуждение
Характерные размеры и морфология адипоцитов. На рисунке, а представлены наиболее характерные типы адипоцитов малого (площадью S =< 300 µm2); среднего (S = 500–900 µm2) и большого (S => 1100 µm2) размеров с различными включениями липидов, полученные из преадипоцитов здоровых животных в культуре 9DIV, растущей на глюкозе. Объем жировых включений увеличивается с ростом размеров клеток в культуре. В малых клетках, содержащих несколько малых жировых капель, объем жировых включений может составить 10–20 % объема цитоплазмы, тогда как в больших – 70–90 % объема цитоплазмы (рисунок, а). На рисунке, б получены культуры из преадипоцитов животных с ожирением. Такие клетки способны накапливать липиды только в присутствии жирных кислот в средах инкубации. У части клеток липидные включения отсутствуют. В других клетках липиды могут занимать до 70–90 % объема цитоплазмы. На рисунке, в представлены зрелые адипоциты животных с D2T. В таких гипертрофированных клетках объем цитоплазмы, не занятой липидными включениями, составляет от 1 до 5 %.
Са2+-сигнализация в адипоцитах здоровых животных. Основные типы периодических и квазипериодических Са2+-колебаний, а также импульсных и триггерных Са2+-ответов, возникающих при аппликации 1–5 мкМ Ach или NE, представлены на рисунке, г–м.
Ранее нами было показано, что культивируемые адипоциты здоровых животных при аппликации Ach или NE (1–10 мкМ) или сыворотки FBS способны генерировать Са2+-колебания различного периода и формы, а также Са2+-импульсы и триггерные переключения, связанные с активацией рианодинового рецептора (RyR) и Са2+-сигнального пути с участием NO/cGMP/cADPr [10] или с вовлечением IP3 рецептора (IP3R) и Са2+-сигнального пути с участием PLC/IP3/IP3R [11].
Включение того или иного Са2+-сигнального пути зависит от типов активируемых рецепторов (α1, α2 или m3) и от наличия L-аргинина в среде инкубации клеток. Влияние размеров клеток на тип генерируемых ответов ранее нами не анализировалось.
а 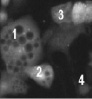 б
б 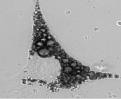 в
в 
г 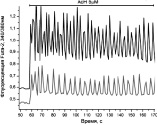 д
д 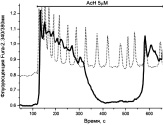
е 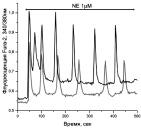 ж
ж 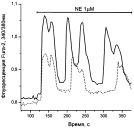 з
з 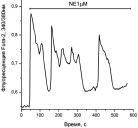
и 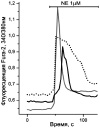 к
к 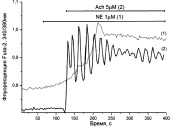 л
л 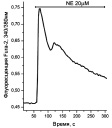
м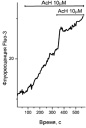
Типы и размеры культивируемых (А, Б) и зрелых (В) адипоцитов и возможные типы Са2 + ответов в них (Г-М) при аппликации Ach, NE. Пояснения на рисунках и в тексте. S – площадь клетки в µm2: а ‒ к онтроль. Адипоцит в клеточной культуре (9DIV). Прокраска Fura-2. S1 = > 1100 µm2; S2,3 = 500-900 µm2. S4 = < 300 µm2; б ‒ ожирение. Адипоцит в клеточной культуре (12DIV). Изображение в проходящем свете. S = > 1100 µm2; в ‒ D2Т. Зрелый адипоцит. Прокраска Hoechst 33342. S = 7850 µm2; г ‒ Ach 5μM. S = < 300 µm2; д ‒ Ach 5μM. S = 500-900 µm2; е – NE 1μM. S = < 300 µm2; ж – NE 1μM. S = 500-900 µm2; з ‒ NE 1μM. S = > 1100 µm2; и ‒ NE 1μM. S = < 300 µm2; к ‒ Ach 5μM. NE 1μM. S = 500-900 µm2; л ‒ NE 20μM. S = > 1100 µm2; м ‒ Ach 10 μM; Ach 10μM. S = 7850 µm2
На рисунке, г представлены «быстрые» Са2+-колебания с периодом от 1 до 10 секунд, наблюдающиеся в клетках малого размера в отсутствие L-аргинина в среде при действии Ach. В таких клетках реже наблюдаются незатухающие колебания с периодом 30–60 секунд (не показано). В клетках среднего и большого размеров наблюдаются колебания с периодами от нескольких десятков до нескольких сотен секунд (рисунок, д). Генерация пачек импульсов с периодом от 1 до 10 секунд с последующей десенситизацией рецепторов и прекращением колебаний, характерна только для клеток малого размера в присутствии Ach. При аппликации NE (1–10 мкМ) в зависимости от размеров клеток возникают устойчивые или затухающие Са2+-колебания с периодами: 15–25 сек (не показано); 50–100 сек (рисунок, е) или несколько минут (рисунок, ж, з). Колебания могут быть простой (рисунок, г, е) или сложной формы (рисунок, ж, з). Наряду с периодическими режимами в культурах 9DIV часть клеток среднего и большого размера может отвечать генерацией одиночных импульсов Са2+(рисунок, и) или триггерным переключением (рисунок, к). Возникновение импульсных или триггерных ответов чаще наблюдается при аппликации NE в сравнении с действием Ach.
Сводные данные о типах ответов при действии Ach и NE приведены в табл. 2. Знаками (+) отмечено наличие у клеток определенных размеров данного типа ответа. Знаками (–) отмечено отсутствие данного типа ответа. Количество знаков (+) указывает на частоту появления соответствующего режима в клетках того или иного размера.
Таблица 2
Типы Са2+-ответов под действием Ach и NE в адипоцитах здоровых животных. Зависимость типа ответа от размеров клетки
|
Площадь клеток (µm2) |
Са2+-колебания (периоды, с) |
Импульсные ответы |
Триггерные переключения |
||||||||
|
1–10 |
15–25 |
50–100 |
100–150 |
200–350 |
|||||||
|
Агонист: 1-5 мкМ Ach |
|||||||||||
|
< 300 |
+++++ |
++ |
– |
– |
– |
– |
– |
||||
|
500–900 |
++ |
++ |
++ |
– |
– |
+ |
+ |
||||
|
> 1100 |
+ |
+ |
++ |
++ |
– |
+ |
+ |
||||
|
Агонист: 1-5 мкМ NE |
|||||||||||
|
< 300 |
– |
++ |
+ |
+ |
– |
++ |
– |
||||
|
500–900 |
– |
+ |
+ |
+ |
_ |
++ |
+ |
||||
|
> 1100 |
– |
– |
+ |
+ |
+ |
++ |
+ |
||||
Из табл. 2 видно, что, как при действии Ach, так и при действии NE, с увеличением размера клеток происходит увеличение периодов генерируемых колебаний. Увеличение размеров клеток приводит также к увеличению вероятности возникновения Са2+-спайков и появления триггерных переключений. В присутствии Ach вероятность возникновения периодических режимов в клетках всех размеров значительно выше, чем при действии NE. Включение L-аргинина в среду инкубации приводит к увеличению периодов колебаний для обоих типов агонистов. Это особенно характерно для клеток малых и средних размеров (не показано).
Са2+-сигнализация в адипоцитах животных с ожирением и D2T. В культивируемых адипоцитах, выделенных из жировой ткани животных с ожирением, представленные на рисунке, г–к типы Са2+-ответов, исчезают. Основным типом ответов становится генерация Са2+-импульсов (рисунок, и), которая возможна только при больших концентрациях Ach или NE (20–30 мкМ). Это может свидетельствовать о наличии резистентности к Ach и NE у животных с ожирением, по крайней мере, применительно к жировой ткани.
Зрелые гипертрофированные адипоциты (S = 5000–10000 µm2), выделенные из жировой ткани животных с D2T, имеют очень малый объём свободной от липидов цитоплазмы (от 1 до 3–5 %, рисунок, в). В таких клетках в малом приядерном слое, в ответ на аппликацию больших концентраций агонистов Ach или NE, возможны импульсы Са2+ малой амплитуды или медленный рост Са2+ (рисунок, м).
Очевидно, что в обоих типах представленных клеток (при ожирении и при D2T) происходит дисрегуляция Са2+-сигнальных систем, связанная с отсутствием условий для формирования положительных обратных связей и генерации Са2+-колебаний с участием IP3R или RyR. Такая дисрегуляция может быть связана с изменением профилей активности и экспрессии различных ферментов и Са2+-каналов основных Са2+-сигнальных путей адипоцитов: PLC/IP3/IP3R/ Са2+-сигнального пути и NO/cGMP/cADPr/RyR/ Са2+-сигнального пути.
Изменения в экспрессии генов при D2T. В табл. 3 представлены данные об экспрессии генов, контролирующих: ключевой фермент цикла Кребса и маркер активности митохондрий (CS); маркер разобщения дыхания митохондрий (UCP-1), а также ключевые ферменты и маркеры липогенеза (GPAT) и липолиза (HSL) и маркеры Са2+-сигнальных путей (IP3R3, RyR2 и PKG1). В табл. 3 – PLC/IP3/IP3R/Ca2+-сигнальный путь представлен в качестве маркера 3 подтипом IP3R, а NO/cGMP/cADPr/RyR/Ca2+-cигнальный путь представлен генами PKG1, CD38 и 2 подтипа рецептора RyR – RyR2.
Таблица 3
Относительная экспрессия мРНК (ΔΔС) ключевых генов в клетках печени и жировой ткани животных с D2T по отношению к экспрессии этих генов у здоровых животных
|
CS |
GPAT |
HSL |
UCP1 |
CD38 |
PKG1 |
IP3R3 |
RyR2 |
|
|
Печень |
0,2 |
0,15 |
0,08 |
1,6 |
0,25 |
0,4 |
1,3 |
0,25 |
|
Жировая ткань |
0,035 |
0,003 |
0,002 |
0,15 |
0,005 |
0,27 |
0,23 |
0,03 |
Примечание. В качестве опорного гена использован ген GAPDH. CS – цитратсинтаза; GPAT – глицерол-3-фосфат-ацилтрансфераза; HSL – гормон чувствительная липаза; UCP-1 – разобщающий дыхание белок; CD38 – АДФ-рибозилциклаза; PKG1 – протеинкиназа G, тип 1; IP3R3 – IP3-рецептор, тип 3; RyR – рианодиновый рецептор, тип 3.
В табл. 3 приведены относительные данные изменения экспрессии генов (мРНК) в гепатоцитах и адипоцитах животных с D2T по отношению к величинам их экспрессии у здоровых животных. Как следует из табл. 3, при D2T происходит 5–10-кратное уменьшение экспрессии мРНК CS, GPAT и HSL в печени, что отражает уменьшение количества митохондрий (CS) при увеличенном разобщении дыхания митохондрий (UCP1); уменьшение активности путей липогенеза (GPAT) и липолиза (HSL). На этом фоне имеет место уменьшение активности Са2+-сигнального пути с участием NO/cGMP/cADPr (уменьшение экспрессии генов CD38 и PKG1) при заметном увеличении активности IP3-зависимого Са2+-сигнального пути (рост экспрессии гена IP3R3).
В клетках жировой ткани при D2T имеет место значительно более сильное уменьшение экспрессии генов (в десятки-сотни раз по сравнению с печенью), как метаболических (CS, GPAT, HSL) так и NO/cGMP/cADPr Ca2+-сигнального пути (при сохранении достаточно высокой экспрессии гена PKG1). В отличие от печени, в жировой ткани экспрессия гена IP3R3 также снижается. Однако такое снижение экспрессии гена IP3R в (4–4,5 раза) выражено значительно меньше, чем уменьшение экспрессии гена RyR (в 30 раз). Наблюдаемое 10–20-кратное снижение экспрессии ключевых метаболических генов (CS, GPAT, HSL) в жировой ткани в сравнении с генами печени означает, что основные метаболические процессы в гипертрофированных адипоцитах (имеющих очень малый объем свободной цитоплазмы) практически подавлены. Основным путем энергопродукции в этих условиях, по-видимому, становится гликолиз, поскольку экспрессия опорного гена GAPDH, характеризующего гликолиз, снижается в 2–3 раза по сравнению с контролем и сравнима с его экспрессией в печени. Очевидно, что такие глобальные перестройки в экспрессии ключевых генов могут приводить к радикальным изменениям в профилях активности экспрессируемых белков, что должно отражаться в изменении условий функционирования (Са2+-ответы, рисунок) и регуляции Са2+-сигнальных путей адипоцитов.
Заключение
Дисфункция жировой ткани и дисреуляция Са2+-сигнальных и метаболических путей гипертрофированных адипоцитов при D2T могут быть связаны с подавлением экспрессии ключевых генов Са2+-сигнальных путей адипоцитов.
Работа выполнена при финансовой поддержке Президиума РАН (программа № 7, проект № 01201258223); ФНМ (проект № 01201256033).
Рецензенты:
Маевский Е.И., д.м.н., профессор, зам. директора Учреждения Российской академии наук Института теоретической и экспериментальной биофизики РАН, г. Пущино;
Мошков Д.А., д.б.н., профессор, зав. лабораторией ультраструктуры нейрона Учреждения Российской академии наук Института теоретической и экспериментальной биофизики РАН, г. Пущино.
Работа поступила в редакцию 27.05.2013.
Библиографическая ссылка
Сергеев А.И., Сирота Н.П., Туровский Е.А., Туровская М.В., Хаустова Я.В., Симонова М.А., Гришина Е.В., Долгачева Л.П., Зинченко В.П., Дынник В.В. ДИСРЕГУЛЯЦИЯ Ca2+-СИГНАЛЬНЫХ ПУТЕЙ АДИПОЦИТОВ ПРИ ОЖИРЕНИИ И ДИАБЕТЕ 2-ГО ТИПА // Фундаментальные исследования. – 2013. – № 6-6. – С. 1436-1441;URL: https://fundamental-research.ru/ru/article/view?id=31755 (дата обращения: 20.04.2024).



