Существующие зарубежные и отечественные суперпластификаторы в отличие от просто пластифицирующих добавок представляют собой в основном синтетические водорастворимые продукты поликонденсации карбо- и гетероциклических соединений с альдегидами, чаще всего с формальдегидом. В результате поликонденсации получают высокомолекулярные соединения, оказывающие пластифицирующее действие на цементные суспензии. Реакция поликонденсации бифункциональных соединений приводит к образованию линейных полимеров, а при конденсации соединений с функциональностью больше двух могут образовываться полимеры с разветвленной и пространственной структурой. При поликонденсации в различных условиях из одних и тех же мономеров могут получаться полимеры с резко различными молекулярными массами, а потому и свойствами. В зависимости от функциональности исходных мономеров и условий реакции при поликонденсации образуются в основном два типа полимеров:
а) линейные – постоянно плавкие растворимые полимеры, не отверждающиеся при нагревании, их называют термопластичными;
б) пространственные – сначала получают плавкие и растворимые низкомолекулярные олигомеры, которые называют термореактивными, затем при нагревании они переходят в неплавкие и нерастворимые состояния, образуя пространственный полимер.
Известные суперпластификаторы, полученные путем поликонденсации, представляют собой термопластичные полимеры. Использование термопластичных полимеров в качестве суперпластификаторов исследовано довольно широко. В то же время в литературе недостаточно данных по применению термореактивных олигомеров для пластификации бетонных смесей. Поэтому их синтез, изучение свойств и строения является актуальным.
Синтез термореактивных олигомеров, многолетние исследования их свойств и влияния на агрегативную устойчивость и пластификацию минеральных суспензий позволили получить соединения, обладающие высокой пластифицирующей активностью [1–7]. Целью данной работы было изучение строения суперпластификаторов на основе оксифенольных олигомеров, полученных при оптимальных условиях синтеза и обладающих наибольшей пластифицирующей способностью.
Для получения термореактивных олигомеров необходимы трифункциональные фенолы. В качестве мономеров были выбраны резорцин и флороглюцин, в качестве конденсирующего агента – формальдегид и фурфурол, катализатором служил едкий натр.
Состав и строение исходных веществ и продуктов реакции определяли методами УФ, ИК-, ПМР-спектроскопии, кондуктометрического титрования, жидкостной хроматографии [2, 7].
Синтез и строение резорцинформальдегидных олигомеров. Схема поликонденсации резорцина с формальдегидом в щелочной среде может быть представлена следующим образом:
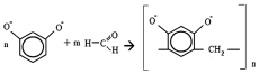
Кинетику получения резорцинформальдегидных олигомеров исследовали с помощью жидкостной хроматографии на хроматографе ХЖ-1305. В качестве адсорбента использовали «ДАУЭКС-Н» фракции 100–150 мкм. Длина колонки 15 см, диаметр 0,1 см, элюент – бидистиллированная вода, скорость потока – 0,125 см3/ч; анализ проводили на длине волны 275 нм, соответствующей максимуму поглощения соединений. В результате реакции получаются термореактивные олигомеры различной молекулярной массы, состав и строение которых определяются соотношением исходных реагентов, их концентрациями и температурой. Изменение температуры значительно влияло на скорость реакции.
В процессе реакции получается смесь олигомеров разной молекулярной массы. Время выхода для жидкостной колоночной хроматографии определяется наличием тех или других функциональных групп. Смесь метилольных производных и олигомеров, имеющих разную молекулярную массу, но одинаковые функциональные группы, выходит одним пиком. В соответствии с этим на хроматограмме наблюдаются два пика, первый из которых соответствует сумме метилольных производных и олигомерных продуктов, второй ‒ резорцину. Изучение зависимости концентрации резорцина и продуктов конденсации от времени синтеза при мольном соотношении формальдегид/резорцин равном 0,82, показало, что концентрация резорцина резко уменьшается и через 5–7 мин достигает практически постоянной величины, составляющей не более 5–8 % от исходной величины. Это объясняется тем, что резорцин расходуется в быстрой реакции образования метилольных производных, в то время как лимитирующей стадией процесса является реакция взаимодействия метилольных соединений друг с другом с образованием молекул олигомеров. Лимитирующая роль реакции образования олигомеров подтверждается также зависимостью молекулярной массы продуктов поликонденсации от времени синтеза. В то время как весовая концентрация продуктов реакции после 5 минут синтеза остается постоянной, молекулярная масса продолжает увеличиваться и только через 40–50 минут ее рост замедляется. Одновременное определение пластифицирующей способности продуктов реакции показало, что вначале молекулярная масса и пластифицирующая способность увеличиваются симбатно, но, начиная с молекулярной массы 750–800, дальнейшее ее возрастание не приводит к росту пластифицирующей способности. Это свидетельствует о том, что увеличение длины цепи олигомерных молекул оказывает влияние на пластифицирующую способность только до определенного предела.
При мольном соотношении около 0,98 образуется высокомолекулярный полимер, нерастворимый в воде. Таким образом, оптимальными условиями синтеза являются: мольное соотношение формальдегид/резорцин 0,82, температура 70 °С, время синтеза 40 мин, загрузка катализатора – 5 % от массы резорцина.
При изучении состава и строения суперпластификатора СБ-Р на основе резорцинформальдегидных олигомеров использовали образец с молекулярной массой 752.
Количество фенольных ОН-групп в молекуле СБ-Р определяли кондуктометрическим методом обратного титрования. Расчет показал, что количество фенольных гидроксильных групп в молекуле олигомера остается неизменным по сравнению с резорцином, следовательно, они не принимают участие в реакции.
Сравнение УФ-спектров СБ-Р и резорцина показало, что характер спектра изменился. Сдвиг R-полосы (28000–36000 см–1) свидетельствует о том, что степень сопряжения в ароматических кольцах олигомерных молекул увеличилась.
Сравнительный анализ ИК-спектров СБ-Р и резорцина показал, что характерным в обоих случаях является отнесение следующих полос поглощения: 1608 см–1, 1500 (валентные колебания С = С кольца), 1370 (валентные колебания С–О фенола), 1295 (колебания ароматического цикла) 1165 (плоскостные деформационные колебания фенольных ОН-групп). Для резорцина наблюдаются также полосы поглощения, характерные для 1,3 – замещения: в области 1900–2000 см–1, а также 850, 773, 680 см–1. В случае СБ-Р эти полосы поглощения исчезают и появляются новые со следующим отнесением: 1450 (деформационные колебания С–Н в СН2-группе), 1227 (деформационные колебания ОН в первичных спиртах), 1085 (валентные колебания С–О в первичных спиртах), 900 (внеплоскостные деформационные колебания С–Н в 1,2,4 и 1,2,4,5-замещенных бензола), 840 (внеплоскостные деформационные колебания СН в 1,2,4-замещенных бензола).
Сравнение ПМР-спектров СБ-Р и резорцина показало, что наблюдается снижение мультиплетности и уменьшение интенсивности сигнала в области 6–7 м.д., обусловленное уменьшением количества протонов в ароматическом кольце. В спектре СБ-Р появляется сигнал в области 3,6 м.д., соответствующий СН2-протонам, связанным с ароматическим кольцом. Изменяется также интенсивность сигнала в области 8 м.д., обусловленного протонами ОН-групп. Интегральная интенсивность ПМР-спектров соответствует предполагаемой структуре соединений. Таким образом, строение молекул СБ-Р в основном можно описать следующей формулой:
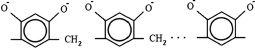
Синтез и строение флороглюцинфурфурольных олигомеров. Реакцию конденсации СБ-ФФ исследовали с помощью ПМР-спектрометра «TESLA BS-476A» с термозондом с рабочей частотой 60 МГц и жидкостного хроматограф с DIFFERENTAL REFRACTOMETER RIDK 101. В качестве адсорбента использовали «SEPARON SC-X C-18», элюентом служила бидистиллированная вода.
Была изучена зависимость концентрации флороглюцина и фурфурола от времени синтеза при оптимальном мольном соотношении реагентов. На дифференциальном ПМР-спектре фурфурола в области 9–10 м.д. имеется пик, образованный в результате резонанса альдегидных протонов фурфурола (рисунок, а).
В ходе реакции поликонденсации путем снятия интегральных кривых определяли зависимость площади этого пика от времени реакции. Изменение площади соответствует изменению относительной концентрации альдегидного протона в реакционной смеси. По мере конденсации менялась форма пика в области 8,0–8,3 м.д., соответствующая протонам –ОН групп флороглюцина. Происходило его расщепление, что соответствует образованию связей:
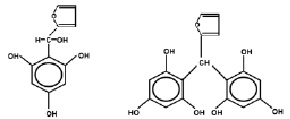
а 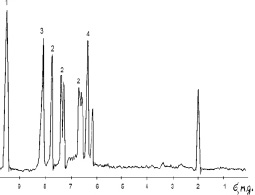 б
б 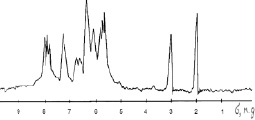
ПМР-спектры: а – смеси флороглюцина и фурфурола; б – СБ-ФФ в дейтероацетоне: 1 – протоны альдегидной группы фурфурола; 2 – протоны фуранового кольца; 3– протоны ОН– групп флороглюцина; 4 – ароматические протоны флороглюцина
В данных соединениях протоны –ОН групп имеют разное окружение и, следовательно, резонируют при разной напряженности внешнего поля. При дальнейшей конденсации наблюдалось более сложное расщепление, т.к. образовывались более сложные структуры олигомеров.
Данные, полученные с помощью хроматографического анализа, показали, что в начале реакции совместной конденсации флороглюцина с фурфуролом образуются их монопроизводные соединения. Вследствие своей высокой растворимости на хроматограмме они выходят раньше других компонентов реакционной смеси. С течением времени наблюдается снижение интенсивности пика флороглюцина и практически полное исчезновение пика фурфурола. Через 40–50 минут происходит дальнейшее изменение структуры молекул, о чем свидетельствует уменьшение пика монопроизводных и пика оставшегося флороглюцина и появление пика олигомеров. Результаты, полученные на ПМР-спектрометре и жидкостном хроматографе, достаточно хорошо соответствуют друг другу.
Схему протекания поликонденсации флороглюцина с фурфуролом в щелочной среде можно представить следующим образом:
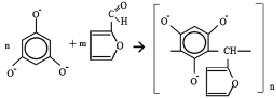
Средняя молекулярная масса при оптимальных условиях синтеза для СБ-ФФ = 950 ± 10.
Строение СБ-ФФ определяли с помощью ИК-спектроскопии на ИК-Фурье-спектрометре Vertex 70, ПМР-спектроскопии и жидкостной хроматографии. Из соотнесения полос поглощения на ИК-спектре сделан вывод, что в спектре СБ-ФФ сохраняются полосы в области 1610 ± 5, 1500 ± 10 см–1 (валентные колебания С = С ароматического кольца); 1370 ± 10 см–1 (валентные колебания С–О фенольные); 1165 ± 10 см–1 (плоскостные деформационные колебания фенольных ОН- групп); 1075 ± 10 см–1 (валентные колебания С–О–С фуранового кольца); а полосы в области 1680 ± 5 см–1 (валентные колебания С = О-карбонильные) исчезают. Появляется интенсивный пик в области 3450 ± 10 см–1 (валентные колебания атомов водорода групп С–Н).
Исследования ПМР-спектров продуктов конденсации показали, что в результате реакции постепенно исчезает сигнал 9–10 м.д., соответствующий протонам альдегидной группы фурфурола и появляется новый пик в области 3 м.д., что свидетельствует о возможном образовании – СН-групп (рисунок). Уширение сигналов ароматических протонов свидетельствует о связи молекул в олигомеры и снижении степени подвижности данных протонов. В области 8 м.д. сохраняется сигнал, соответствующий протонам ОН-групп флороглюцина. Один сигнал расщепляется на несколько, что соответствует изменению влияния соседних протонов в результате появления дополнительных заместителей в ароматических кольцах флороглюцина.
На основании данных ИК-спектороскопии, ПМР-спектроскопии, жидкостной хроматографии и кондуктометрического титрования (расчет показал, что в среднем в одной молекуле содержится 18 ± 0,5 фенольных ОН- групп [2]) можно предположить как наиболее вероятную следующую схему Н-формы молекулы СБ-ФФ.
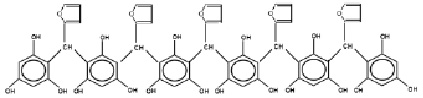
Олигомеры СБ-ФФ получали и использовали в дальнейшем в виде натриевых солей, хорошо растворимых в воде.
Определены оптимальные условия синтеза, методами ИК-, ПМР-спектроскопии, хроматографии, кондуктометрии и другими установлены состав и строение термореактивных олигомеров СБ-Р и СБ-ФФ. Известно, что получение термопластичных олигомеров протекает, как правило, в кислой среде. В связи с этим возникает необходимость нейтрализации продуктов реакции, получение же термореактивных олигомеров идет в щелочной среде, причем при более мягких условиях.
Рецензенты:
Евтушенко Е.И., д.т.н., профессор, проректор по научной работе, ФГБОУ ВПО «Белгородский государственный технологический университет им. В.Г. Шухова», г. Белгород;
Павленко В.И., д.т.н., профессор, директор института строительного материаловедения и техносферной безопасности, ФГБОУ ВПО «Белгородский государственный технологический университет им. В.Г. Шухова», г. Белгород.
Работа поступила в редакцию 25.12.2013.
Библиографическая ссылка
Полуэктова В.А., Шаповалов Н.А., Балятинская Л.Н. СИНТЕЗ И СТРОЕНИЕ СУПЕРПЛАСТИФИКАТОРОВ НА ОСНОВЕ ОКСИФЕНОЛЬНЫХ ОЛИГОМЕРОВ // Фундаментальные исследования. – 2013. – № 11-6. – С. 1136-1141;URL: https://fundamental-research.ru/ru/article/view?id=33263 (дата обращения: 25.04.2024).



