Уникальные свойства вещественного состава и строения алюмосиликатных полых микросфер, получаемых из отходов сжигания углей на тепловых электростанциях, определили широкий круг их использования в производстве керамических легковесных теплоизоляционных материалов, радиопрозрачных керамик, облегчённых тампонажных смесей и буровых растворов. [1–4]. Из микросфер можно спекать прочные агломераты, которые являются прекрасными теплоизоляторами, не уступающими по своим свойствам пенопласту. Более того, теплоизоляция из микросфер выдерживает температуры до 1000–1200 °С, в то время как пенопласт начинает плавиться при 300 °С. Испытания показали также высокую эффективность применения микросфер в химической промышленности в качестве наполнителя для различных полимерных материалов, в том числе сферопластиков и термопластиков.
За рубежом область применения полых микросфер также достаточно широка: они входят в состав стеклопластиков в комбинации со стекловолокном, заливочных паст для заделки швов (пазов, пустот), синтетических пен, высококачественных лёгких бетонов с улучшенными тепло- и звукоизоляционными характеристиками. На основе тугоплавких микросфер в США изготавливались теплозащитные керамические плитки для обшивки космических аппаратов многоразового использования. Вовлечение микросфер в сферу промышленного производства приводит к снижению стоимости продукции, увеличению её прочностных, электрических, тепловых и звукоизоляционных и других высокотехнологичных свойств, способствующих дальнейшему росту перспективных направлений утилизации СПМ и развитию минерально-сырьевой базы данного вида техногенного сырья. Если обобщить полученные данные, можно сделать вывод о том, что суммарное количество ACM, ежегодно образующихся на крупных электростанциях, составляет около 120 тыс. т. Согласно технико-экономическим расчётам, при создании установки при одной ТЭС с объёмом производства ACM в 2000 т в год экономический эффект может составить 1,5–2,5 долларов США в год в зависимости от её регионального расположения.
Авторами данной статьи впервые разработаны катализаторы на базе ценосфер для очистки дымовых газов ТЭС от NOx, SO2, CO. [5] В настоящем сообщении приведены результаты структурирования и стабилизации железо-молибденовых катализаторов окисления метанола до формальдегида в присутствии микросфер энергетических зол ТЭС.
Цель исследования – разработка и исследование наноразмерных, стабилизированных микросферическими алюмосиликатными катализаторами окисления метанола.
Результаты исследования и их обсуждение
Методически для классификации летучей золы от сжигания Экибастузского угля использовали колонный пульсационный аппарат диаметром 50 мм с пневматическими пульсаторами и завихряющими перегородками. Расстояние между перегородками составляло 80 мм, а площадь живого сечения насадки – 30 %. Скорость восходящего потока воды составляла 0,005 м/с. Амплитуду пульсации выдерживали в пределах 5 мм. Частоту пульсации варьировали в пределах отношений: плотность/ удельная поверхность, присущих двум немагнитным продуктам (кварцевый песок и g-Al2O3). В данном случае 0,2–5,0 имп./мин. В нижней части колонны расположили кольцевой электромагнит, обеспечивающий требуемый диапазон напряжённости магнитного поля в сечении восходящего потока (1000 Гс). Эффективность процесса определяли визуальным контролем за качеством выделенных продуктов с использованием электронного микроскопа. Параллельные пробы выборочно подвергали рентгенофазовому анализу. Выход полых микросфер определяли после осаждения суспензии верхнего слива колонны в отстойнике. В зависимости уровня ввода исходной суспензии выход полых микросфер составил соответственно 51, 82, 84, 88, и 89 %.
Микросферические алюмосиликатные катализаторы готовили на основе микросфер (ценосфер), выделенных из летучих зол энергетических углей. В данной работе сбор микросфер осуществляется с поверхности воды пруда-накопителя золоотвала ТЭЦ-2 (Алматы), работающей на углях Экибастузского месторождения. Фазовый состав микросфер представлен в основном кварцем и муллитом. Размеры микросфер варьируются от 150 до 250 мкм, предел прочности на сжатие 150–280 кг/см2, твёрдость по шкале Мооса – 5–6.
Типичные микроснимки выделенных алюмосиликатных микросфер представлены на рис. 1.
Химический состав (табл. 1) представлен оксидами алюминия, кремния, железа, кальция и титана (~95 масс %).
Для изучения микросферических композиций мы использовали спектральные методы. На рис. 2 представлен ИК-спектр исследуемых алюмосиликатных композитов. Наблюдается интенсивная полоса поглощения в интервале частот 1200–1000 см–1. Этот интервал частот характерен для групп Si–O, Al–O, Si–O–Al: n–1100, 1066, 1022, 1050, 900 см–1. Полосы поглощения в низкочастотной области спектра от 668 до 614 см-1 относятся к Fe–O в группе Fe2O3.
Для исследования форм и состояния железа в составе стекол (магнитоупорядоченные фазы и твердые растворы с участием катионов Fe 3 + ) успешно применяется метод ЭПР. В типичном спектре ЭПР ценосфер наблюдается узкая линия с g-фактором 4,3, а также широкая линия, являющаяся суперпозицией двух симметричных сигналов с g-факторами 2,20–2,06 (I) и 2,2–2,3 (II).
В соответствии с литературными данными сигнал в области с g = 4,3 следует приписать одиночным ионам Fe3+ , находящимся в кристаллических полях низкой симметрии и, в частности, в силикатных стеклах. Широкие сигналы I и II связаны с присутствием в ценосферах магнитоупорядоченных фаз, обуславливающих появление ферримагнетизма. Такими фазами в ценосферах могут являться кристаллические соединения со структурой шпинели в двух крайних формах: твердые растворы на основе магнетита Fe3O4, присутствие которого обнаружено в наиболее магнитных образцах методом РФА, а также феррита Mg или Mn (g = 2,2–2,10). В связи с тем, что реальный состав этих фаз, скорее всего, соответствует твердым растворам на их основе, то обозначения Fe3O4 (магнетит) и MeFe2O4 (шпинель) используются в дальнейшем достаточно условно.

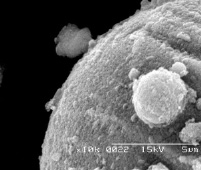
Рис. 1. Электронные микрофотографии алюмосиликатных микросфер, выделенных из золы ТЭЦ-2 г. Алматы
Таблица 1
Элементный и химический состав алюмосиликатных микросфер (ценосфер), масс. %
|
Образец |
Al2O3 |
SiO2 |
CaO |
TiO2 |
Fe2O3 |
Na2O |
S |
P |
SrO |
ZrO |
|
Исход. |
26,4 |
59,73 |
2,15 |
1,13 |
5,51 |
0,82 |
0,187 |
0,599 |
0,0407 |
0,0532 |
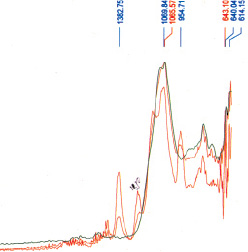
Рис. 2. ИК-спектр микросферических алюмосиликатов, выделенных из золы ТЭЦ-2 г. Алматы
В области малых содержаний железа (до 3–4 масс. % Fe2O3) две вышеуказанные линии (g = 2,0–2,3) являются близкими к симметричным (суперпарамагнитное состояние). С увеличением содержания железа в ценосферах появляется дополнительное поглощение в области низких магнитных полей, приводящее к анизотропии сигнала магнитного резонанса. При рассмотрении особенностей ферримагнитных фаз возможны следующие варианты:
1) размеры отдельных частиц этих фаз меньше типичных размеров доменов (монодоменное приближение);
2) размеры отдельных частиц больше размера отдельного домена, характерного для данных фаз (полидоменное приближение).
В первом случае используются различные подходы для описания спектров электронного магнитного резонанса отдельного домена. Феноменологический подход связан с описанием движения магнитного момента во внешних магнитных полях в целом. При этом в зависимости от соотношения энергий теплового движения частиц и анизотропного взаимодействия магнитного момента с внешним полем возможно усреднение анизотропии частицы (явление «суперпарамагнетизм») или появление анизотропной уширенной линии.
Данные ЭПР показывают, что железо (3+) находится в основном в двух формах: одиночные ионы Fe3+ в стекле и в частицах магнитоупорядоченной фазы шпинельной структуры размером 30–50 Å при содержании железа 3–4 масс. % Fe2O3. При содержании железа в ценосферах ниже 2 масс. % Fe2O3 железо (3+) находится преимущественно в форме одиночных ионов.
Мессбауэровские исследования ценосфер показали, что в ценосферах с содержанием более 7 масс. % Fe2O3 железо входит в состав двух фаз – дефектного магнетита (67 %) и фазы, по параметрам близкой к разупорядоченному ортосиликату монтичеллита (Ca, Mg, Fe)2SiO4 (33 %). Дефектный магнетит при комнатной температуре находится в двух магнитных равнозаселенных состояниях: ферримагнитное и суперпарамагнитное. Подрешетки магнетита разбавлены диамагнитным замещением. Диамагнитное разбавление и малый размер шпинельных образований приводит к суперпарамагнитному состоянию и разрушению быстрого электронного обмена между ионами Fe3+ и Fe2+ в В-подрешетки магнетита.
Ценосферы с меньшей концентрацией Fe2O3 (3–4 масс. %) содержат железо в составе шпинели (47 %) и ортосиликата (53 %). Шпинель находится в парамагнитном состоянии при комнатной температуре. В силикате железо в двухвалентном состоянии занимает октаэдрическую позицию типа М2.
На основе анализа результатов можно отметить следующие особенности суперпарамагнитной фазы железа по сравнению с магнетитом.
Железо смешанной валентности не обнаружено. Вероятно, быстрый электронный обмен Fe3+ ↔ Fe2+ , свойственный стехиометрическому магнетиту, разрушается совместным действием диамагнитного разбавления и дефектностью малых шпинельных областей.
Из изменения заселенностей позиций железа при уменьшении концентрации железа в ценосферах следует, что катионы Fe3+ обогащают тетраэдрическую подрешетку, вытесняя Al3+ в октаэдрическую подрешетку.
Ионы Fe3+ , обнаруженные методом ЭПР в стеклофазе в виде одиночных центров, вероятно, имеют малую заселенность и/или параметры их сверхтонкой структуры близки к параметрам Fe3+ в шпинели (рис. 3).
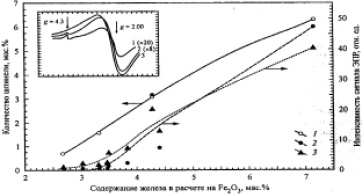
Рис. 3. Зависимость содержания шпинельных фаз в ценосферах по данным ЭПР
По данным термодинамических расчетов, электронного парамагнитного резонанса и Мессбауэровской спектроскопии ценосфер энергетических зол установлено, что железо входит в состав ценосфер в двух состояниях – Fe3+ и Fe2+ , при этом в области содержания железа 3–4 масс. % Fe2O3 железо (3 +) находится преимущественно в двух формах – одиночных ионов в стекле и частиц суперпарамагнитной фазы со структурой шпинели размером 30–50 Å, диспергированных в алюмосиликатном стекле. Подрешетки суперпарамагнитной шпинели диамагнитно разбавлены ионами Al3+ . Ценосферы с содержанием более 7 маcс. % Fe2O3 имеют в своем составе также магнитную фазу на основе дефектного магнетита.
Вышеприведенные результаты свидетельствуют о том, что в микросферах, выделенных из зол ТЭЦ-2, уже содержится железо, причем наноструктурированное. Пропитывание микросфер молибдатом аммония приводит к формированию железо-молибденового катализатора.
Полученные катализаторы обладают высокой механической прочностью. Элементный и химический анализ, проведённый с использованием рентгенофлуоресцентного спектрометра PhilipsPW2400 показал следующий состав (табл. 2).
Таблица 2
Элементный и химический анализ катализатора, масс. %
|
Наименование |
SiO2 |
Al2O3 |
Fe2O3 |
MoO3 |
Na2O |
|
Железо-молибденовый алюмосиликатный катализатор |
50,0–60,0 |
25,0–35,0 |
3,5–5,5 |
7,0–15,0 |
4,5–4,0 |
В ИК-спектрах алюмосиликатного катализатора наблюдаются интенсивные полосы поглощения, характерные для групп S–O, Al–O, Si–O–Al. Полосы поглощения в низкочастотной области спектра указывают на присутствие Fe3+ и W6+ в оксидах. Удельная поверхность катализаторов, вычисленная по полным изотермам низкотемпературной адсорбции азота по методу БЭТ, измеренной на приборе BelSorp (BelJapanInc.), составляет 14,7–15,8 м2/г. Интегральный объём пор катализатора, прокаленного при 400 °C, составляет 0,57 мл/г. Оптимальный размер активных частиц разработанных катализаторов – 40–50 нм.
Полученные катализаторы испытаны в процессе окисления метанола до формальдегида. Эксперимент проводили в автоматизированном универсальном проточном каталитическом реакторе – ПКУ-1. Одновременный анализ всех компонентов парогазовой смеси проводили на газохроматографическом комплексе на базе хроматографа «ХРОМОС ГХ-1000». (Разработка и производство – ООО «СOЛО» / ООО «Центр «ХромоСиб»). Результаты представлены в табл. 3–6.
Таблица 3
Влияние соотношения Mo/Fe на активность микросферического алюмосиликатного катализатора в процессе окисления метанола до формальдегида. PO2 = 13 %, удельная поверхность катализатора – 12,6 м2/г, T = 640 K. Скорость газового потока – 0,34 л/мин
|
Соотношение Mo/Fe |
Содержание метанола в смеси, % |
Степень превращения метанола, % |
Выход формальдегида, % |
Селективность окисления метанола в формальдегид, % |
|
1,1 |
6,5 |
91,8 |
90,2 |
98,3 |
|
1,5 |
6,5 |
93,6 |
92,85 |
99,2 |
|
2,0 |
6,5 |
96,2 |
96,1 |
99,9 |
|
2,2 |
6,5 |
97,3 |
95,15 |
97,8 |
|
2,5 |
6,5 |
98,4 |
93,7 |
95,2 |
Полученные результаты свидетельствуют о том, что в интервале Mo/Fe от 1,1 до 2,0 наряду с повышением степени превращения метанола, выхода формальдегида повышается и селективность окисления метанола в формальдегид.
Дальнейшее повышение соотношения Mo/Fe мало отражается на степени превращения метанола, но понижается выход формальдегида и, как следствие, селективность процесса. В продуктах реакции обнаружены: муравьиная кислота (до 3,4 %) и оксид углерода (до 1,3 %).
Повышение содержания метанола в смеси от 4,2 до 6,0 % приводит к росту практически до 100 % степени превращения метанола, выходу формальдегида и селективности процесса.
Таблица 4
Влияние содержания метанола в смеси на степень превращения метанола, выход формальдегида и селективность окисления метанола в формальдегид в присутствии микросферического алюмосиликатного катализатора. PO2 = 13 %, удельная поверхность катализатора – 12,6 м2/г, T = 640 K, скорость газового потока – 0,34 л/мин, Mo/Fe – 2,0
|
Содержание метанола в смеси, % |
Степень превращения метанола, % |
Выход формальдегида, % |
Селективность окисления метанола в формальдегид, % |
|
4,2 |
94,54 |
92,3 |
97,6 |
|
5,1 |
96,75 |
95,1 |
98,3 |
|
6,0 |
99,3 |
99,3 |
100 |
|
8,0 |
99,4 |
98,11 |
98,7 |
|
10,0 |
99,5 |
97,0 |
97,5 |
При дальнейшем повышении содержания варьируемого компонента наблюдается некоторый спад контролируемых параметров и появление небольшого количества примесей муравьиной кислоты (до 2,4 %).
Таблица 5
Влияние скорости подачи газовой смеси метанол ‒ кислород ‒ азот на степень превращения метанола, выход формальдегида и селективность окисления метанола в формальдегид в присутствии микросферического алюмосиликатного катализатора. PO2 = 13 %, удельная поверхность катализатора – 12,6 м2/г, содержание метанола в смеси – 6,0 %, кислорода – 9,0 %, T = 540 K, Mo/Fe – 2,0
|
Скорость газового потока, мл/мин |
Степень превращения метанола, % |
Выход формальдегида, % |
Селективность окисления метанола в формальдегид, % |
|
210,0 |
96,8 |
96,4 |
99,6 |
|
250,0 |
97,9 |
97,7 |
99,8 |
|
340,0 |
99,9 |
99,9 |
100,0 |
|
450,0 |
99,8 |
99,8 |
100,0 |
|
550,0 |
99,7 |
99,7 |
100,0 |
|
600,0 |
99,8 |
99,8 |
100,0 |
Из приведенных данных видно, что в интервале скорости газового потока CH3OH–O2–N2 от 210 до 340 мл/мин повышаются основные параметры.
Таблица 6
Влияние времени работы катализатора на его активность. PO2 = 13 %, удельная поверхность 14,7 м2/г для микросферического алюмосиликатного катализатора, T = 640 K, скорость потока CH3OH–O2–N2 – 0,34 л/мин, Mo/Fe = 2,0
|
Продолжительность работы катализатора, ч |
Метанол на входе, % |
Степень превращения метанола, % |
Выход формальдегида, % |
Селективность окисления метанола в формальдегид, % |
|
40 |
6,1 |
98,8 |
98,3 |
97,8 |
|
80 |
7,5 |
98,7 |
96,6 |
99,6 |
|
122 |
9,1 |
98,6 |
98,2 |
99,6 |
|
482 |
10,1 |
98,7 |
98,2 |
99,5 |
|
674 |
9,1 |
98,8 |
98,8 |
100,0 |
|
729 |
7,5 |
98,8 |
98,8 |
100,0 |
Результаты, приведенные в табл. 6, свидетельствуют о том, что силикатный катализатор во времени деградирует при повышении содержания метанола на входе до 9,0 % и возвращается к исходному значению при понижении содержания метанола до 6,12. В то же время алюмосиликатный катализатор стабилен на всем протяжении времени работы не зависимо от содержания метанола на входе.
Таким образом, полученные результаты показали, что оптимальными условиями окисления метанола в присутствии алюмосиликатного микросферического катализатора являются: соотношение Mo/Fe > 2, содержание метанола в исходной смеси CH3OH-O2-N2 – 6,0–10,0 %, кислорода – 9,0–13 %, скорость газового потока 600 мл/. В оптимальных условиях степень превращения метанола находится на уровне 99,8 % при 100 % селективности превращения его в формальдегид.
Рецензенты:
Наурызбаев М.К., д.т.н., профессор, директор ДГП на ПХВ Центр физико-химических методов исследования и анализа РГП на ПХВ, «КазНУ им. аль-Фараби» Министерства образования и науки РК, г. Алматы;
Досумов К.Д., д.х.н., профессор, заместитель директора ДГП на ПХВ Центр физико-химических методов исследования и анализа РГП на ПХВ «КазНУ им. аль-Фараби» Министерства образования и науки РК, г. Алматы.
Работа проступила в редакцию 02.06.2014.
Библиографическая ссылка
Емельянова В.С., Емельянова В.С., Шакиева Т.В., Шакиева Т.В., Шакиев Э.М., Шакиев Э.М., Досумова Б.Т., Досумова Б.Т., Джаткамбаева У.Н., Джаткамбаева У.Н., Айбульдинов Е.К., Айбульдинов Е.К. ИСПОЛЬЗОВАНИЕ ЗОЛЫ УНОСА ТЕПЛОВЫХ ЭЛЕКТРОСТАНЦИЙ ДЛЯ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ОКИСЛЕНИЯ МЕТАНОЛА В ФОРМАЛЬДЕГИД // Фундаментальные исследования. – 2014. – № 9-6. – С. 1230-1236;URL: https://fundamental-research.ru/ru/article/view?id=35044 (дата обращения: 23.04.2024).



