Ранее, используя логико-структурный подход, а также прогностические компьютерные программы, нами были обоснованы структуры целевых соединений и на этой основе осуществлен целенаправленный синтез новых гетерилзамещённых 2,3-дигидро-1H-хиназолин-4-онов. Для полученных соединений с помощью программы PASS были выявлены 8 видов активности с вероятностью от 30 до 92 %, однако максимально вероятной (до 92 %) оказалась противовоспалительная активность. Поэтому дальнейшие фармакологические исследования были осуществлены именно в этом направлении [1–5].
Целью нашего исследования является молекулярное моделирование и изучение противовоспалительной активности гетерилзамещённых 2,3-дигидро-1H-хиназолин-4-онов.
Материалы и методы исследования
С целью изучения степени сродства лиганд-фермент нами проведены расчеты энергии взаимодействия в лиганд-белковом комплексе с использованием молекулярного докинга. На модели «ватной гранулемы» оценена противовоспалительная активность исследуемых соединений.
Результаты исследования и их обсуждение
Известно, что данные, полученные на основе программы PASS, могут служить лишь ориентировочной характеристикой при отборе вероятных лидеров среди прогнозируемых структур. Поэтому экспериментально на модели «ватной гранулемы» нами изучено противовоспалительное действие синтезированных соединений.
Исследование проведено на 54 крысах-самках линии Wistar весом 180–200 г (на момент начала эксперимента).
Белых крыс вводили в состояние хлоралгидратного сна (доза 350 мг/кг), и в области спины выстригалась шерсть. В асептических условиях делался разрез кожи и подкожной клетчатки длиной около 1 см, после чего пинцетом в подкожной клетчатке через разрез формировалась полость, куда помещался простерилизованный ватный шарик массой 15 мг, а затем на рану накладывалось два шва. В течение всего опыта (7 суток) крысам в пищевод при помощи зонда вводили исследуемые соединения. Подопытных животных разделили на 9 групп по 6 особей в каждой: 1 группа – контрольная, которой вводили физиологический раствор; животным 2-й группы вводили препарат сравнения – диклофенак (в дозе, соответствующей в пересчете на массу взрослого человека); группам 3–9 – вводили исследуемые вещества в виде суспензий (в дозе 50 мг/кг). На восьмые сутки опыта имплантированный шарик с образовавшейся вокруг него грануляционной тканью извлекался, взвешивался, затем высушивался до постоянной массы при 60–65 °С. О величине экссудативной фазы воспаления судили по разнице масс (мг) шарика до и после высушивания, о величине пролиферативной фазы – по разнице в массе (мг) высушенного шарика с его исходной массой 15 мг. Данные представлены в табл. 1.
Таблица 1
Результаты определения противовоспалительной активности гетерилпроизводных 2,3-дигидро-1H-хиназолин-4-онов
|
Объект |
Экссудация, мг |
Пролиферация, мг |
|
Контроль |
202,0 ± 6,6# |
34,0 ± 2,2# |
|
Диклофенак |
183,0 ± 2,7* |
30,0 ± 1,7* |
|
1(QFur) |
117,0 ± 14,4*# –36 % < PD –42 % < PK |
25,0 ± 3,5*# –17 % < PD –26 % < PK |
|
2(QFurI) |
112,0 ± 11,4*# –39 % < PD –45 % < PK |
26,0 ± 1,6*# –13 % < PD –24 % < PK |
|
3(QFurMe) |
147,0 ± 7,2*# –20 % < PD –27 % < PK |
35,0 ± 2,2 +17 % > PD +3 % > PK |
|
4(QFurBenzNO2) |
117,0 ± 6,7*# –36 % < PD –42 % < PK |
25,0 ± 3,3*# –17 % < PD –26 % < PK |
|
5(QDzPh) |
138,0 ± 10,0*# –25 % < PD –32 % < PK |
28,0 ± 1,8* –7 % < PD –18 % < PK |
|
6(QDzBenz) |
155,0 ± 19,0* –15 % < PD –23 % < PK |
30,0 ± 6,0 0 % = PD –12 % < PK |
|
7(QFurIsoInd) |
190,0 ± 14,1 +4 % > PD –6 % < PK |
42,0 ± 4,6# +40 % > PD +24 % > PK |
Примечания:
* – достоверно по отношению к контролю (*P < 0,05);
# – достоверно по отношению к диклофенаку (#P < 0,05);
PD – процент относительно диклофенака;
PK – процент относительно контроля.
Как видно из данных табл. 1, вещества 1–6 относительно диклофенака снижают достоверно эксудацию соответственно на 36; 39; 20; 36; 25; 15 %. Соединение 7 на уровне диклофенака влияет на стадию экссудации. Соединения 1, 2, 4, 5 снижают пролиферацию достоверно по отношению к диклофенаку на 17; 13; 17; 7 %. Соединение 3 по сравнению с диклофенаком увеличивает пролиферацию на 17 %, а 7 на 40 %.
Относительно контрольной группы достоверное снижение экссудации показывают соединения 1–5 на 42; 45; 27; 42; 32 %. Пролиферация относительно контрольной группы достоверно снижается под влиянием соединений 1, 2, 4 соединения на 26; 24; 26 % соответственно. Соединение 3 действует на уровне контроля, а 7 – увеличивает пролиферацию на 24 %.
Используя молекулярное моделирование при помощи программы Molegro Virtual Docker (версия 5.5), был осуществлен расчет степени сродства молекул к таким ферментам-мишеням, как циклооксигеназа-1 и циклооксигеназа-2, играющим ключевую роль в механизмах воспаления. Поскольку эти два основных подтипа фермента в разной степени участвуют в процессах воспаления, мы сочли целесообразным сопоставить энергии докинга для обоих из них. Данные представлены в табл. 2.
Таблица 2
Энергии взаимодействия гетерилзамещённых 2,3-дигидро-1H-хиназолин-4-онов с ЦОГ-1 и ЦОГ-2
|
Лиганд/Фермент |
ЦОГ 1 |
ЦОГ 2 |
|
1 QFur |
– 98,52 (+26 %) |
–93,97 (+78 %) |
|
2 QFurI |
–102,59 (+31 %) |
–63,16 (+39 %) |
|
3 QFurMe |
–91,38 (+17 %) |
–78,34 (+73 %) |
|
4 QFurBenzNO2 |
–95,32 (+22 %) |
–81,18 (+79 %) |
|
5 QDzPh |
–83,57 (+7 %) |
–50,40 (+11 %) |
|
6 QDzBenz |
–86,26 (+10 %) |
–55,12 (+22 %) |
|
7 QFurIsoInd |
–79,20 (+1 %) |
–48,45 (+7 %) |
|
Диклофенак |
–78,15 (±0) |
–45,29 (±0) |
Примечание. (+ %) – прирост в % относительно энергии связывания с диклофенаком.
Диклофенак обладает выраженными анальгезирующим и противовоспалительным свойствами: неизбирательно угнетая ферменты ЦОГ-1 и ЦОГ-2, он нарушает метаболизм арахидоновой кислоты и синтез простагландинов.
Одним из важных факторов, влияющих на уровень фармакологического эффекта, является энергия связывания лиганда с рецептором/ферментом: чем ниже энергия связывания, тем прочнее лиганд-ферментный комплекс и тем вероятнее эффект будет сильнее.
Мы сочли целесообразным изучить взаимосвязь между энергией докинга (в процентном соотношении с диклофенаком) и фармакологическим действием (экссудация и пролиферация относительно диклофенака). Для этого мы создали модель, в которой контрольная группа была принята за 0 %. Отправным значением, взятым за 100 %, служил препарат сравнения – диклофенак.
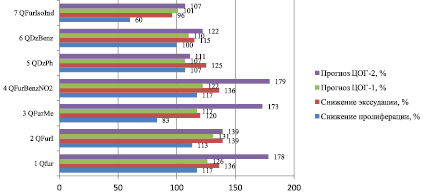
Взаимосвязь энергии докинга с ЦОГ-1/ЦОГ-2 в % и степень экссудации и пролиферации в %
Из данного графика видно, что наименьшей энергией докинга с ЦОГ-2 характеризуются соответственно соединения 1–4. Энергии взаимодействия с ЦОГ-1 незначительны. Можно предположить, что противовоспалительное действие исследуемого ряда соединений обусловлено ингибированием в большей степени фермента ЦОГ-2.
Выводы
- Молекулярный докинг новых гетерилзамещённых 2,3-дигидро-1H-хиназолин-4-онов показывает что, вероятнее всего, исследуемые соединения в большей степени ингибируют ЦОГ-2 и в меньшей мере ЦОГ-1.
- Фармакологические исследования новых гетерилзамещённых 2,3-дигидро-1H-хиназолин-4-онов на модели «ватной гранулемы» подтверждают данные молекулярного докинга.
- Соединения 1, 3, 6 являются лидерами по противовоспалительной активности и превосходят по действию препарат сравнения – диклофенак. Их можно рекомендовать для дальнейших углубленных фармакологических исследований.
Рецензенты:
Попова О.И., д.фарм.н., профессор кафедры фармакогнозии, Пятигорский медико-фармацевтический институт, филиал ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск;
Погорелый В.Е., д.б.н., профессор кафедры фармакологии с курсом клинической фармакологии, Пятигорский медико-фармацевтический институт, филиал, ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.
Работа поступила в редакцию 23.07.2014.
Библиографическая ссылка
Бандура А.Ф., Оганесян Э.Т., Кодониди И.П., Сергеева Е.О., Саджая Л.А., Сочнев В.С., Золотых Д.С., Луговой И.С., Базганов А.Ю. О ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТИ НОВЫХ ГЕТЕРИЛЗАМЕЩЕННЫХ ПРОИЗВОДНЫХ 2,3-ДИГИДРО-1H-ХИНАЗОЛИН-4-ОНА // Фундаментальные исследования. – 2014. – № 9-6. – С. 1260-1263;URL: https://fundamental-research.ru/ru/article/view?id=35050 (дата обращения: 17.04.2024).



