Гестозы занимают второе место в статистике акушерских осложнений [3]. Их патогенез окончательно не изучен, а диагностика и прогнозирование до настоящего времени представляют собой трудную задачу [5].
В последние годы была экспериментально доказана связь между ишемией плаценты и повреждением эндотелия, вначале – в зоне маточно-плацентарного кровообращения, а затем – генерализованно. Авторы указывают на возможную связь между повышенным уровнем плацентарных изоферментов ЩФ и уровнем плацентарной недостаточности [6].
Плацентарная щелочная фосфатаза (ПЩФ) продуцируется микроворсинками плаценты и эндотелием её новообразующихся сосудов, является органоспецифическим антигеном плаценты, в связи с чем логично предположить непосредственное участие этого фермента в указанных патологических процессах.
Исследованию ПЩФ как маркера эмбриональных и малигнизированных тканей, в последние десятилетия уделено большое внимание [8]. Однако в тени ПЩФ остаются другие ферменты этого органа, обладающие фосфатазной активностью.
Целью нашей работы стало комплексное исследование активности и концентрации щелочных фосфатаз в ткани плаценты здоровых женщин и при гестозах.
В работе использованы экстракты 14 плацент, полученных при нормальных родах, и 48 плацент, полученных при родах женщин, страдавших гестозами.
Для приготовления водно-солевого экстракта кусочки плаценты гомогенизировали до однородной массы, добавляя при этом 10 mM Tris-HCl, буфер pH 7,4 в соотношении 1:4. Гомогенат центрифугировали и надосадочную жидкость использовали для исследования.
Для приготовления бутанольного экстракта осадок, полученный на 1 этапе, ресуспендировали в 10 mM Tris-HCl, буфер pH 7,4, содержащем бутанол (20 %,v/v), и перемешивали в течении 6–8 часов при температуре –2–4 °С. Через сутки указанную смесь центрифугировали с эфиром в течение 40–45 минут при 10000 об/мин в рефрижераторной центрифуге 2–3 раза в соотношении I часть эфира и 5 частей гомогената. После центрифугирования отделяли водную фазу, определяли общий белок и активность щелочной фосфатазы в надосадочной жидкости.
Активность щелочной фосфатазы определяли по расщеплению n-нитрофенилфосфата и нафтол-AS-фосфата, а количество органоспецифической плацентарной фосфатазы определяли методом ракетного электрофореза. Активность термостабильной плацентарной щелочной фосфатазы определяли после термической обработки водно-солевых и бутанольных экстрактов.
В водно-солевых экстрактах послеродовой плаценты содержится от 512 до 2048 МЕ общей активности щелочной фосфатазы и от 2048 до 4096 МЕ – в бутаноловых экстрактах. По нашим данным, использование субстратов n-нитрофенилфосфата и нафтол-AS-фосфата не оказывает достоверного влияния на уровень активности общей щелочной фосфатазы плаценты, и далее мы не акцентируем внимание на субстратной специфичности. Выявленная активность общей плацентарной щелочной фосфатазы соответствует 7,6 ± 1,0 МЕ/100 г ткани в водно-солевых экстрактах и 22,8 ± 3,0 МЕ/100 г – в бутаноловых экстрактах плаценты. То есть существует цитозольная (вероятно, она же – секретируемая в кровоток) плацентарная щелочная фосфатаза и мембраносвязанная плацентарная щелочная фосфатаза, обеспечивающая метаболизм фетоплацентарного комплекса.
В водно-солевых экстрактах плаценты при гестозах отмечается достоверное снижение активности термостабильной щелочной фосфатазы (табл. 1). Причем характерно значительное снижение различия между уровнем щелочной фосфатазы в водно-солевых и бутанольных экстрактах (более чем на 42 %). Наблюдается опережающее снижение уровня именно мембраносвязанного фермента, что, видимо, усугубляет функциональное состояние фетоплацентарного комплекса.
Таблица 1
Активность термостабильной щелочной фосфатазы в экстрактах плаценты здоровых женщин и страдающих гестозом
|
Донор плаценты |
Водно-солевой экстракт МЕ |
Бутанольный экстракт МЕ |
|
Здоровые женщины (n = 14) |
1316,57 ± 108,5 |
3120,27 ± 142,7 |
|
Женщины, страдавшие гестозом (n = 48) |
998,55 ± 112,8 |
1677,57 ± 156,6 |
Получение поликлональных антител к очищенному препарату плацентарной щелочной фосфатазы позволило разработать моноспецифическую тест-систему на этот фермент.
Плацентарная щелочная фосфатаза по данным двумерного иммуноэлектрофореза состоит из 2-х иммунохимически идентичных компонентов с относительной электрофоретической подвижностью 0,65 ± 0,04 и 0,52 ± 0,02, что соответствует описанным в литературе [Mosbah A.A., 2011] F и S изоформам (рис. 1). Прогревание при 56 °С в течение 30 минут или 60 °С – 10–15 минут сохраняет активность ПЩФ, что свидетельствует о её основном отличии от других изоформ ЩФ свойстве – термостабильности .
В работе использован препарат плацентарной щелочной фосфатазы полученный в лаборатории кафедры химии Астраханской медицинской академии.
С помощью очищенного препарата ПЩФ нами были получены гипериммунные сыворотки к этому белку, которые позволили разработать методы количественного определения ПЩФ в экстрактах плаценты, используя минимальное количество биоматериала.

Рис. 1. Двумерный иммуноэлектрофорез экстракта плаценты. F-фракция с электрофоретической подвижностью 0,65, S-фракция с электрофоретической подвижностью 0,52. Агароза содержит антитела к плацентарной щелочной фосфатазе
Для количественного определения ПЩФ использовали метод ракетного иммуноэлектрофореза (РИЭФ). Метод предполагает использование калибровочного графика при каждом анализе. В качестве стандартного образца используют одну из серий очищенного препарата ПЩФ.
Для стандартизации в этом случае может быть использован очищенный лиофилизированный ПЩФ: его раствор приготовлен по точной навеске. Однако разные серии ПЩФ различаются между собой в пределах ошибки препаративных методов, а образцы кроличьей сыворотки отличаются по концентрации антител, а это может влиять на результаты определения содержания ПЩФ методом РИЭФ.
На рис. 2 представлена типичная электрофореграмма данного эксперимента. С помощью программы Excel для каждого образца строили график зависимости «ПЩФ – высота «ракеты» и находили уравнение линейной регрессии. Для оценки значимости различий линий регрессии применяли регрессионный анализ, заключающийся в сравнении коэффициентов наклона b, коэффициентов сдвига a, сравнения двух линий в целом (по F-критерию) [1].
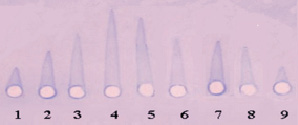
Рис. 2. Типичная электрофореграмма при определении пщф; 1–4 – Разведения ПЩФ. Концентрации 5; 10; 15; 20 мкг/мл; 5, 6, 7, 8, 9 – образцы тканей плаценты
Таблица 2
Концентрация плацентарной термостабильной щелочной фосфатазы в экстрактах плаценты здоровых женщин и страдающих гестозом
|
Донор плаценты |
Водно-солевой экстракт мкг/100 г ткани |
Бутанольный экстракт мкг/100 г ткани |
|
Здоровые женщины (n = 18) |
1017,517 ± 14,5 |
2176,6 ± 42,1 |
|
Женщины, страдавшие гестозом (n = 48) |
804,11 ± 12,3 * |
1836,8 ± 26,0* |
Примечание. * – P ≤ 0,01.
На этих условиях было проведено 17 опытов ракетного иммуноэлектрофореза, в которых испытано 136 образцов ткани плацент и образцов биологических жидкостей.
В водно-солевых экстрактах плаценты при гестозах отмечается достоверное (более 20 %) снижение концентрации ПЩФ, а бутанольных чуть менее 16 % (табл. 2). Причем наблюдается заметное отличие в динамике изменений концентрации плацентарной щелочной фосфатазы, определенной иммунохимическими методами и изменения активности термостабильной щелочной фосфатазы (табл. 3).
Таким образом, на основании исследования водно-солевых и бутаноловых экстрактов послеродовой плаценты мы пришли к выводу, что существует цитозольная (вероятно, она же – секретируемая в кровоток) плацентарная щелочная фосфатаза и мембраносвязанная плацентарная щелочная фосфатаза, обеспечивающая метаболизм фетоплацентарного комплекса. Дисбаланс динамики активности термостабильной щелочной фосфатазы и концентрации специфической плацентарной щелочной фосфатазы подтверждает не только факт значительного присутствия фосфатаз различного происхождения в водно-солевой фракции, но и следует признать, что специфическая плацентарная фосфатаза не единственная мембрансвязанная фосфатаза.
Интересно, что снижение концентрации менее выражено (табл. 3), чем снижение активности. Расчет удельной активности валовой термостабильной щелочной фосфатазы показывает, что в нормально развивающейся плаценте в водно-солевых экстрактах удельная активность щелочной фосфатазы составляет 1,3 ± 0,02 ед./мкг плацентарной щелочной фосфатазы, а в бутанольных экстрактах 1,43 ± 0,02 ед./мкг ПЩФ. В плацентах, полученных от женщин, страдавших гестозом, удельная активность щелочной фосфатазы в водно-солевых экстрактах составляет 1,18 ± 0,025 ед./мкг ПЩФ, а в бутанольных экстрактах 0,91 ± 0,01 ед./мкг ПЩФ. Анализ этих данных показывает, что самое значительное снижение удельной активности происходит при сравнении бутанольных экстрактов нормальной плаценты и плаценты женщин, страдавших гестозами. Здесь различие составляет более 36 %.
Таблица 3
Сравнительная активность плацентарной термостабильной щелочной фосфатазы в экстрактах плаценты здоровых женщин и страдающих гестозом
|
Донор плаценты |
Водно-солевой экстракт |
Бутанольный экстракт |
||||
|
Активность ТЩФ МЕ |
Концентрация ПЩФ, мкг/100 г ткани |
Удельная активность, ед./мкг |
Активность ТЩФ МЕ |
Концентрация ПЩФ, мкг/100 г ткани |
Удельная активность, ед./мкг |
|
|
Здоровые женщины (n = 21) |
1316,57 ± 108,5 |
1017,517 ± 14,5 |
1,3 ± 0,02 |
3120,27 ± 142,7 |
2176,6 ± 42,1 |
1,43 ± 0,02 |
|
Женщины, страдавшие гестозом (n = 33) |
998,55 ± 112,8 |
804,11 ± 12,3 |
1,18 ± 0,025 |
1677,57 ± 156,6 |
1836,8 ± 26,0 |
0,91 ± 0,01 |
В нормальной плаценте отмечено недостоверное различие в удельной активности щелочной фосфатазы в водно-солевых и бутанольных экстрактах, несмотря на то, что при определении активности щелочной фосфатазы в водно-солевых и бутанольных экстрактах эти различия очень значительны и составляют более 230 %. Это кажущееся противоречие можно объяснить примерно равноценной долей специфической плацентарной фосфатазы в общем фосфатазном пуле как водно-солевого, так и бутанольного экстрактов. Эту точку зрения подтверждает и наблюдение Zhabin S.G., Луценко М.Т [9,2]
Резкое снижение на 36 % удельной активности в бутанольных экстрактах плаценты женщин, страдавших гестозами, по сравнению с нормальной плацентой, свидетельствует об опережающем снижении уровня специфической плацентарной фосфатазы в мембрансвязанной фракции, а значительное увеличение различия между удельной активностью щелочной фосфатазы в водно-солевых и бутанольных экстрактах (более чем на 23 %) может свидетельствовать в пользу представления о более активном вымывании именно специфической плацентарной фосфатазы в цитозольную фракцию [4].
Следовательно, при гестозах происходит не только количественное изменение уровня плацентарной щелочной фосфатазы, но и, во-первых, дисбаланс между цитозольной и мембранной фракциями щелочной фосфатазы и, во-вторых, изменение профиля многочисленных фосфатаз, клеток плаценты, с опережающим снижением уровня специфической плацентарной щелочной фосфатазы, что усугубляет функциональное состояние фетоплацентарного комплекса.
Рецензенты:
Мажитова М.В., д.б.н., доцент, зав. кафедрой химии фармацевтического факультета ГБОУ ВПО «Астраханская государственная медицинская академия», г. Астрахань;
Молдавская А.А., д.м.н., профессор кафедры анатомии человека, ГБОУ ВПО «Астраханская государственная медицинская академия», г. Астрахань.
Работа поступила в редакцию 21.12.2013.



