Бурное развитие фармацевтической отрасли в последнее десятилетие сопровождается образованием и накоплением фармацевтических отходов. Попадание в окружающую природную среду высокостабильных, токсичных фармполлютантов, которые характеризуются не только необычностью структуры, но и высокой биологической активностью ингредиентов, крайне нежелательно даже в относительно низких концентрациях [7]. Продолжительное выделение фармпрепаратов и их метаболитов в сточные воды может приводить к их аккумуляции и тем самым стимулировать отрицательное воздействие этих химических соединений на окружающую среду [10]. Одним из наиболее часто обнаруживаемых в сточных, грунтовых, поверхностных водах (и даже питьевой воде) лекарственных препаратов является широко применяемый в медицинской практике парацетамол (N–(4-гидроксифенил)ацетамид) [7, 10]. Парацетамол обладает выраженным обезболивающим и антипиретическим действием. Из-за своих физико-химических свойств (наличие бензольного кольца, замещенного гидроксильной группой и ацетаминогруппой в пара (1,4)-положении) парацетамол потенциально персистентен, мобилен в водных и сухопутных экосистемах [10, 13].
В ранее проведённых нами исследованиях установлена способность актинобактерий Rhodococcus ruber разрушать химическую структуру парацетамола [3]. В процессе ферментолиза парацетамола в культуральной среде родококков были идентифицированы п-аминофенол, гидрохинон, пирокатехин, муконовая кислота. Процесс биодеструкции парацетамола сопровождался постепенным приобретением культуральной средой коричневой окраски и последующим образованием гидрофобного темноокрашенного (благодаря присутствию хиноидных соединений) круповидного, оседающего на дно колбы осадка. Массовая доля выхода осадка от исходного количества парацетамола составляла 20 %. Жидкость над осадком оставалась прозрачной. Формирование этого осадка, возможно, связано с высокой адгезивной активностью родококков в отношении парацетамола, усиленным синтезом внеклеточных полимеров, а также полимеризацией интермедиатов (фенольных и хиноидных соединений) бактериальной деструкции парацетамола. С использованием метода солевой агрегации показано, что родококки формируют клеточные агрегаты под действием сравнительно низких (0,2−0,4 М) концентраций сульфата аммония, что свидетельствует о выраженной гидрофобности их клеточной стенки [5]. Возможность полимеризации продуктов деградации парацетамола при участии пероксидазы хрена подтверждена исследованием D.W. Potter с соавт. [12]. В работах P. Kar с соавт. [8, 9] рассмотрена окислительная полимеризация о-, м- и п-аминофенола и представлены результаты определения средней молекулярной массы поли-м-аминофенола [8].
Цель настоящего исследования − определение средней молекулярной массы осадка, образующегося в результате биодеструкции парацетамола клетками R. ruber ИЭГМ 77.
Материалы и методы исследования
В работе использовали штамм R. ruber ИЭГМ 77 из Региональной профилированной коллекции алканотрофных микроорганизмов (официальный акроним коллекции ИЭГМ, номер во Всемирной федерации коллекций культур (WFCC) #768) [14]. Парацетамол в виде фармацевтической субстанции (Аньцю Луань Фармасьютикал Ко., Лтд., Китай) вносили в среду культивирования родококков до конечной концентрации 2000 мг/дм3. Эксперименты по биодеструкции парацетамола проводили в условиях периодического культивирования клеток R. ruber ИЭГМ 77 при 28 °С в течение 20 сут [3]. Образовавшийся осадок (ОО) отфильтровывали, трижды промывали дистиллированной водой и высушивали до постоянной массы.
Содержание воды в ОО определяли на анализаторе влажности МА-30 (Sartorius, Германия). Элементный анализ (С, Н, N) выполняли с помощью элементного анализатора Leco CHNS-9321P (Leco Europe B.V., Нидерланды). Результаты элементного анализа корректировали с учётом влажности и зольного остатка, полученного в результате “мокрой” минерализации ОО [1].
Среднюю молекулярную массу ОО определяли методами гель-проникающей хроматографии и капиллярной вискозиметрии. Для определения средней молекулярной массы ОО вискозиметрическим методом готовили серию растворов ОО в ДМСО в диапазоне концентраций от 0,0125 до 0,0500 г/см3. Полученные растворы фильтровали через стеклянный фильтр с диаметром пор 100–160 мкм. Удельную вязкость (ηуд) растворов и растворителя определяли, измеряя время их истечения в капиллярном вискозиметре с диаметром капилляра 0,56 мм в соответствии с методикой [2] по формуле
ηуд = (t – t0)/t0,
где t – время истечения раствора ОО, с; t0 – время истечения растворителя, с.
Объём растворителя и растворов ОО составлял 10,00 см3 при температуре 20 °С. Расчёт средней молекулярной массы ОО осуществляли по уравнению Марка-Куна-Хаувинка [2]:
[η] = K∙Mα, (1)
где α – константа, характеризующая форму макромолекулы в растворе; K – константа для данного гомологического ряда полимеров и растворителя. Параметры K и α в формуле (1) рассчитывали по данным работ P. Kar с соавт. [8, 9] и N. Naar с соавт. [11].
Для определения средней молекулярной массы ОО методом гель-проникающей хроматографии использовали Sephadex G-100 с диаметром частиц 40–120 мкм (Pharmacia Fine Chemicals, Швеция), имеющий пределы фракционирования 4000–150000 Да. Хроматографическую колонку размерами 30,0×1,5 см заполняли гелем сефадекса, предварительно подготовленным согласно методике [4]. Объём геля сорбента составлял 46,8 см3 при высоте наполнения в колонке 26.5 см. В качестве элюента использовали 0,1 М раствор NaOH. Исследуемым образцом являлся 0,25 % раствор ОО в 0,1 М растворе NaOH. Нанесение образца на гель в объеме 0,20 см3 и хроматографирование осуществляли в соответствии с методиками [4]. Скорость фильтрации составляла 0,1 см3/мин. Для сбора фракций использовали стеклянные пикнометры вместимостью 2,00–10,00 см3. Детектирование фракций осуществляли в диапазоне длин волн 200–700 нм на спектрофотометре Lambda EZ 201 (Perkon Elmer, CША). Полученные данные использовали для построения трехмерного графика, отражающего зависимость между оптической плотностью (A), объемом выхода фракций (Vl) и длиной волны (λ).
Подбор аналитической длины волны, необходимой для определения объема выхода элюата, соответствующего средней молекулярной массе ОО, выполняли по градуировочному графику зависимости A (λ) для серии растворов ОО в 0,1 М растворе NaOH в диапазоне концентраций от 0,0500 до 0,2500 г/см3. Растворы ОО фильтровали через бумажные обеззоленные фильтры.
Расчет средней молекулярной массы ОО осуществляли по стандартной формуле [4]:
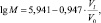 (2)
(2)
где Vl – объем выхода элюата, соответствующий точке максимума на трехмерном графике зависимости A (Vi, λ) при выбранной длине волны, см3; V0 – объем растворителя между гранулами геля («свободный» растворитель), см3. Объем растворителя между гранулами рассчитывали, исходя из характеристик набухания Sephadex G-100 в воде и объема геля в колонке [4].
Результаты исследования и их обсуждение
На рис. 1 представлен график линейной зависимости приведенной вязкости (ηуд/c) от концентрации растворов ОО. Значение характеристической вязкости [η], полученное посредством экстраполяции линии тренда на ось ординат, равно 5,1 см3/г.
Значения K и α в формуле (1) для определения средней молекулярной массы ОО неизвестны. По данным N. Naar с соавт., значение α для полианилина, являющегося своеобразным «химическим каркасом» полиаминофенолов, составляет 0,73 [11]. Значение K зависит от природы полимера и растворителя [6]. Так, по данным P. Kar с соавт., для одного из продуктов полимеризации м-аминофенола получены значения характеристической вязкости [η] его растворов в ДМСО и средней молекулярной массы, равные 203,0 см3/г и 100000 Да, соответственно [8]. На основании результатов исследований P. Kar с соавт. [8] и N. Naar с соавт. [11] нетрудно найти искомое значение K в формуле (1) для определения средней молекулярной массы ОО:
K = 203,0/1000000.73 = 0,0455.
Таким образом, средняя молекулярная масса ОО, рассчитанная по уравнению 5,1 = 0,0455∙M0,73, равна 643,16 Да.
Для определения средней молекулярной массы ОО наряду с капиллярной вискозиметрией использовали метод гель-хроматографии. Как видно из рис. 2, на трехмерном графике зависимости A(Vl, λ) отмечаются два пика при длинах волн 218 и 318 нм, которые соответствуют объему выхода элюата 50,00 см3.
Для выбора аналитической длины волны далее были построены графики зависимости оптической плотности от длины волны растворов ОО в диапазоне концентраций (c) от 0,0500 до 0,2500 г/см3. Как видно из рис. 3, во всех электронных спектрах отмечаются максимумы поглощения при длинах волн 218 и 318 нм.
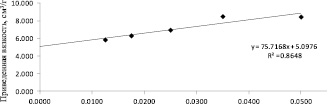
Рис. 1. Зависимость приведённой вязкости от концентрации раствора ОО
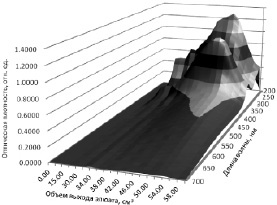
Рис. 2. Трехмерный график зависимости оптической плотности полученных фракций от объема выхода элюата и длины волны
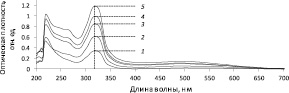
Рис. 3. Спектры поглощения растворов ОО с различными концентрациями: 1 – 0,0500 г/см3; 2 – 0,1000 г/см3; 3 – 0,1500 г/см3; 4 – 0,2000 г/см3; 5 – 0,2500 г/см3
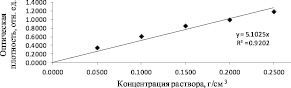
Рис. 4. Градуировочный график зависимости оптической плотности от концентрации раствора ОО при длине волны 318 нм
Линейная зависимость A (c) проявляется при λmax = 318 нм (рис. 4).
Коэффициент перехода (L) от оптической плотности к концентрации раствора ОО при 318 нм равен 5,1025. Содержание ОО (мкг) во фракциях, собранных в процессе гель-фильтрации, рассчитывали, исходя из полученного значения коэффициента L.
Распределение содержания ОО во фракциях № 5–19 представлено на рис. 5.
Как видно из рис. 5, максимальное содержание ОО отмечается во фракции № 14, соответствующей объему выхода элюата 50,00 см3.
По данным гель-фильтрации, средняя молекулярная масса ОО, рассчитанная по формуле (2), составляет 5973,55 Да. Данное значение значительно отличается от результатов (643,16 Да), полученных с использованием метода капиллярной вискозиметрии. Это находит объяснение в использованных нами расчетных формулах. При определении средней молекулярной массы ОО методом гель-хроматографии применяли уравнение для расчета средней молекулярной массы глобулярных белков. Следовательно, для сравнения использованных нами методов необходимо внести поправку в значение α, равное 0,73 [11], использованное нами при определении средней молекулярной массы ОО вискозиметрическим методом, и приблизить его к значению 0,50, соответствующему полимерам со сферической формой молекул [6]. С учетом поправки при K = 0,0455 и M = 5973,55 Да параметр α становится равным 0,5429, что подтверждает результаты определения средней молекулярной массы ОО методом гель-хроматографии.
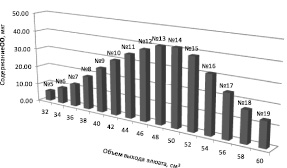
Рис. 5. Распределение содержания ОО во фракциях
Элементный состав ОО и поли-м-аминофенола
|
Объект анализа |
С |
H |
N |
O + S |
|
ОО |
48,45 |
4,83 |
10,17 |
36,56 |
|
Поли-м-аминофенол |
52,75 |
4,85 |
10,25 |
32,20 |
Результаты элементного анализа ОО, представленные в таблице, сопоставимы с теоретическими значениями содержания C, H, N в поли-м-аминофеноле [8].
Заключение
Средняя молекулярная масса (5973,55 Да) осадка, образующегося в культуральной жидкости Rhodococcus ruber ИЭГМ 77 в процессе биодеструкции парацетамола, установленная с помощью методов гель-фильтрации и капиллярной вискозиметрии, свидетельствует о полимерной природе продукта. Исходя из предложенных путей биодеструкции парацетамола [3, 15] и данных элементного анализа, в качестве одного из потенциальных мономеров может рассматриваться производное п-аминофенола.
Дальнейшие исследования осадка, образующегося в результате биодеструкции парацетамола клетками R. ruber ИЭГМ 77, будут посвящены установлению его структуры.
Исследования выполнены при частичной поддержке Программы ОБН РАН № 12 «Живая природа: современное состояние и проблемы развития» (проект № 15-12-4-10) и гранта Российского научного фонда (№ 14-14-00643).
Рецензенты:
Ярыгина Т.И., д.фарм.н., профессор кафедры фармацевтической химии, ГБОУ ВПО «ПГФА» Минздрава России, г. Пермь;
Михайловский А.Г., д.фарм.н., профессор кафедры общей и органической химии, ГБОУ ВПО ПГФА Минздрава России, г. Пермь.



