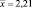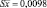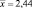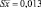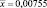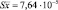Многие препараты, используемые для коррекции патологических состояний печени, не лишены побочных эффектов, что особенно опасно при длительном приёме. Предпочтение здесь следует отдавать комплексным препаратам растительного происхождения, способным нормализовать метаболизм, функции и структуру паренхимы печени, стимулирующим синтез нуклеиновых кислот и белка, а также обладающих холекинетическими и иммуномодулирующими свойствами [3]. В этом плане наше внимание привлекли препараты расторопши пятнистой, бессмертника песчаного и биомасса гриба Fusarium sambucinum (Милайф®).
Нами разработан состав и технология таблеток, покрытых пленочной оболочкой, включающих порошок биомассы Fusarium sambucinum, сухие экстракты расторопши пятнистой и бессмертника песчаного (условное название «Рабемил») [4].
Целью работы явилась разработка методик идентификации и количественного определения основных биологически активных веществ в таблетках, включающих порошок биомассы Fusarium sambucinum, сухие экстракты расторопши пятнистой и бессмертника песчаного, покрытых пленочной оболочкой.
Материалы и методы исследования
В работе использовались спектрофотометрические и хроматографические методы анализа, установленные требованиями Государственной фармакопеи ХI и ХII изданий, а также Европейской фармакопеи [1, 2, 5].
Результаты исследования и их обсуждение
Первым этапом работы явилось определение подлинности флавоноидов в экстракте цветков бессмертника песчаного сухом и экстракте расторопши сухом
Для определения флавоноидов в экстрактах были использованы химические и физико-химические методы.
Качественная реакция:
К 0,05 г экстракта прибавляли 1 мл спирта этилового 95 % в 0,1 г порошка магния, 1 мл кислоты хлористоводородной концентрированной. Наблюдали постепенное появление красного окрашивания.
Спектры поглощения
Изучение спектров поглощения спиртового раствора экстрактов бессмертника песчаного и расторопши пятнистой показало, что из-за перехода в экстракт суммы действующих веществ, извлекаемых из исходного сырья, УФ-спектр имеет полосы поглощения, которые трудно отнести к полосам конкретных действующих веществ. Для большей достоверности использовали дифференциальные спектры поглощения комплекса суммы флавоноидов бессмертника и расторопши с алюминия хлоридом. Оба спектра характеризуются полосой поглощения в области 410 ± 2 нм.
Для получения дифференциальных спектров 0,5 г экстракта вносили в мерную колбу вместимостью 25 мл, доводили до метки спиртом этиловым 95 %-ным, фильтровали. В две мерные колбы вместимостью 25 мл вносили по 1 мл фильтрата для экстракта бессмертника или 2 мл экстракта расторопши. В первую колбу прибавляли 10 мл спирта этилового 95 % и 2 мл 2 % спиртового раствора алюминия хлорида. Через 10 минут добавляли 0,1 мл кислоты уксусной разведенной, доводили до метки спиртом этиловым 95 % (раствор А). Во вторую колбу прибавляли 10 мл спирта этилового 95 % и 0,1 мл кислоты уксусной разведенной, доводили до метки спиртом этиловым 95 % (раствор Б).
Через 30 минут измеряли оптическую плотность раствора А на спектрофотометре СФ-56 в кювете с толщиной слоя 1 см. В качестве раствора сравнения использовали раствор Б.
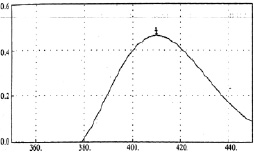
Рис. 1. Спектр поглощения 0,002 % раствора стандартного образца (СО) рутина
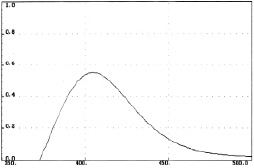
Рис. 2. Спектр поглощения флавоноидов продукта взаимодействия сухого экстракта бессмертника песчаного с алюминия хлоридом
Нами были измерены дифференциальные спектры поглощения комплекса суммы флавоноидов цветков бессмертника песчаного, расторопши и комплекса рутина с алюминием хлоридом. Все три спектра близки по положению максимумов (рис. 1, 2, 3).
Основными действующими веществами семян расторопши являются флавоноиды и флавонолигнаны (силибин, силикристин, силидианин и др.). Содержание флаволигнанов в смесях в пересчете на СО силибин осуществляется методом спектрофотометрии при длине волны 289 нм (рис. 3).
Однако на спектре поглощения имеется максимум в более длинноволновой области (рис. 4).
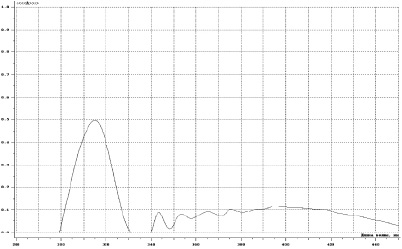
Рис. 3. Спектр поглощения флавоноидов продукта взаимодействия сухого экстракта расторопши с алюминия хлоридом
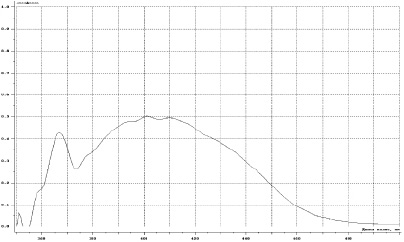
Рис. 4. Спектр поглощения флавоноидов продукта взаимодействия сухого экстракта расторопши с алюминия хлоридом в длинноволновой области спектра
Так как перед нами стояла задача определения суммы флавоноидов в таблетках, содержащих экстракты расторопши и бессмертника песчаного, то в качестве стандарта использовали рутин, который чаще других применяется при количественном определении суммы флавоноидов в растительном сырье.
Хроматографический анализ
Для идентификации флавоноидов в экстрактах использовали хроматографию в тонком слое сорбента. На линию старта наносили 1 мкл раствора экстракта, 0,002 % раствор СО рутина в спирте этиловом 95 %, раствор СО лютеолина в спирте этиловом 95 % и раствор СО изосалипурпозида в спирте этиловом 95 %. Хроматографировали восходящим способом в системе растворителей: бутанол-1 – кислота уксусная ледяная – вода (4:1:5), детектировали в УФ-свете (365 нм).
Экстракт цветков бессмертника песчаного
На хроматограмме раствора испытуемого образца на уровне СО изосалипурпозида обнаружили пятно желто-бурого цвета [Rf 0,80 ± 0,05]. На уровне СО лютеолина также обнаружили пятно желто-бурого цвета [Rf 0,95 ± 0,03]. Оба пятна после обработки раствором алюминия хлорида 2 % в спирте этиловом 95 % приобрели ярко-желтое окрашивание (рис. 5).
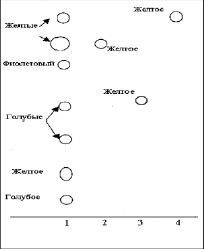
Рис. 5. Хроматограмма флавоноидов в экстракте бессмертника: 1 – 0,01 % раствор экстракта бессмертника песчаного; 2 – 0,002 % раствор СО изосалипурпозида; 3 – 0,002 % раствор СО рутина; 4 – 0,002 % раствор СО лютеолина
Таким образом, растворы СО изоалипурпозида и лютеолина могут быть использованы для идентификации флавоноидов цветков бессмертника песчаного.
Так как в настоящее время изосалипурпозид – стандарт на территории Российской Федерации не выпускается, дополнительно в качестве стандартного образца был использован один из наиболее доступных в настоящее время флавоноидов – рутин. Значение Rs пятна изосалипурпозид (извлечение), рассчитанное относительно рутина (Rf 0,56 ± 0,02), составило 1,47.
Экстракт расторопши
На хроматограмме раствора испытуемого образца на уровне СО лютеолина и СО рутина обнаружены пятна желто-бурого цвета. Оба пятна после обработки раствором алюминия хлорида 2 % в спирте этиловом 95 % приобрели ярко-желтое окрашивание (рис. 6).
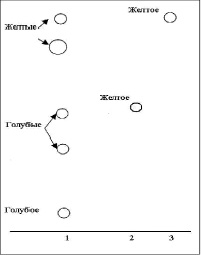
Рис. 6. Хроматограмма флавоноидов экстракта расторопши: 1 – 0,01 % раствор экстракта расторопши; 2 – 0,002 % раствор СО рутина; 3 – 0,002 % лютеолина
Определение содержания суммы флавоноидов в экстрактах цветков бессмертника песчаного сухого и расторопши
Для выполнения анализа 0,5 экстракта вносили в мерную колбу вместимостью 25 мл, доводили спиртом этиловым 95 %-ным до метки, фильтровали, отбрасывали первые порции фильтрата. В две мерные колбы вносили по 1 мл фильтрата и далее поступали, как описано в методике определения подлинности суммы флавоноидов спектрофотометрическим методом.
Параллельно с измерением исследуемых растворов измеряют оптическую плотность раствора СО рутина.
В мерные колбы вместимостью 25 мл помещают по 1 мл раствора СО рутина, далее поступают, как указано в методике выше.
Приготовление 0,002 % раствора СО рутина. Около 0,05 г (точная навеска) СО рутина растворяли в спирте этиловом 95 %, в мерной колбе вместимостью 100 мл; охлаждали, доводили объем раствора тем же растворителем до метки.
Содержание суммы флавоноидов в пересчете на рутин (Хг, га 100 г экстракта) рассчитывали по формуле
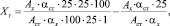
где Ах – оптическая плотность исследуемого раствора; Аст – оптическая плотность СО раствора рутина; αст – навеска СО рутина, г; αх – навеска сухого экстракта бессмертника или расторопши.
Результаты определения суммы флавоноидов в экстракте цветков бессмертника песчаного сухом в пересчете на рутин приведены в табл. 1.
Таким образом, содержание флавоноидов в 100 г экстракта цветков бессмертника песчаного в пересчете на рутин составляет 2,21 г ± 0,025 %. Относительная погрешность определения ± 1,15 %.
Результаты определения суммы флавоноидов в экстракте расторопши сухом в перечете на рутин приведены в табл. 2.
Таким образом, содержание флавоноидов в экстракте расторопши в пересчете на рутин составляет 2,44 ± 0,034. Относительная погрешность определения ± 1,38 %
Определение содержания суммы флавоноидов в таблетках
Для выяснения влияния на спектр поглощения порошка Милайфа и вспомогательных веществ, входящих в состав таблеток, готовили модельную смесь без экстрактов цветков бессмертника песчаного и расторопши, измеряли спектр поглощения после добавления раствора алюминия хлорида. Оказалось, что при данном разведении оптическая плотность практически равнялась нулю.
Таким образом, милайф и вспомогательные вещества не мешают определению суммы флавоноидов в таблетках.
Для выполнения анализа 0,5 г (точная навеска) порошка растертых таблеток вносили в мерную колбу вместимостью 25 мл, добавляли 15 мл спирта этилового 95 %, перемешивали, доводили тем же растворителем до метки, фильтровали, отбрасывали первые порции фильтрата. В две мерные колбы вносили по 2 мл фильтрата и далее поступали, как описано в методике определения подлинности суммы флавоноидов спектрофотометрическим методом.
Таблица 1
Результаты количественного определения суммы флавоноидов в экстракте цветков бессмертника песчаного сухом (Аст = 0,430)
|
Навеска (г) |
Ах |
Найдено флавоноидов, % |
Метрологические характеристики |
|
0,5040 |
0,385 |
2,224 |
|
|
0,4911 |
0,377 |
2,235 |
S = 0,241 |
|
0,4859 |
0,368 |
2,202 |
|
|
0,5062 |
0,386 |
2,217 |
Δх = 0,0252 |
|
0,5121 |
0,382 |
2,169 |
х ± Δх = 2,21 ± 0,025 |
|
0,4960 |
0,380 |
2,227 |
ε = ± 1,15 % |
Таблица 2
Результаты количественного определения суммы флавоноидов в экстракте расторопши сухом (Аст = 0,430)
|
Навеска (г) |
Ах |
Найдено флавоноидов г/100 г экстракта |
Метрологические характеристики |
|
0,5145 |
0,429 |
2,423 |
|
|
0,4958 |
0,423 |
2,480 |
S = 0,032 |
|
0,4983 |
0,413 |
2,412 |
|
|
0,4837 |
0,400 |
2,406 |
Δх = 0,082 |
|
0,5074 |
0,432 |
2,473 |
х ± Δх = 2,44 ± 0,034 |
|
0,5179 |
0,437 |
2,455 |
ε = ± 1,38 % |
Таблица 3
Результаты количественного определения суммы флавоноидов в таблетках (Аст = 0,430)
|
Навеска (г) |
Ах |
Найдено флавоноидов, г |
Метрологические характеристики |
|
0,5143 |
0,385 |
0,0075 |
|
|
0,5090 |
0,377 |
0,0078 |
S = 1,87∙10–4 |
|
0,4915 |
0,368 |
0,0074 |
|
|
0,5121 |
0,386 |
0,0077 |
Δх = 4,87∙10-4 |
|
0,4935 |
0,382 |
0,0073 |
х ± Δх = 0,0075 ± 1,76∙10–4 |
|
0,4991 |
0,380 |
0,0076 |
ε = ± 2,60 % |
Параллельно с измерением исследуемых растворов измеряют оптическую плотность 0,002 % раствора СО рутина.
В мерные колбы вместимостью 25 мл помещают по 1 мл раствора СО рутина, далее поступают, как указано в методике выше.
Содержание суммы флавоноидов в таблетке пересчете на рутин (Хг) рассчитывали по формуле

где Ах – оптическая плотность исследуемого раствора; Аст – оптическая плотность СО раствора рутина; αст – навеска СО рутина, г; αх – навеска порошка растертых таблеток, г; Р – средняя масса таблетки, г.
Результаты определения суммы флавоноидов в таблетках в пересчете на рутин приведены в табл. 3.
Таким образом, содержание флавоноидов в таблетках в пересчете на рутин составляет 0,0075 г ± 1,76∙10–4. Относительная погрешность определения ± 2,60 %.
Выводы
1. Разработаны методики качественного и количественного анализа основных биологически активных веществ таблеток, включающих порошок биомассы Fusarium sambucinum, сухие экстракты расторопши пятнистой и бессмертника песчаного.
2. Для определения флавоноидов в экстрактах использовали метод дифференциальной спектрофотометрии и хроматографию в тонком слое сорбента, где в качестве стандартных образцов использовали изосалипурпозид, лютеолин и рутин.
3. Для количественного определения содержания суммы флавоноидов в экстрактах цветков бессмертника песчаного сухого и расторопши использовали спектрофотометрию в видимой области (длина волны – 410 нм) по реакции с алюминия хлоридом (стандартный образец – рутин). Нормы качества разработанных таблеток установлены согласно требованиям Государственной фармакопеи РФ ГФ ХI и ХII изданий, а также Европейской фармакопеи.
Рецензенты:
Сампиев А.М., д.фарм.н., профессор, зав. кафедрой фармации, ГБОУ ВПО «Кубанский государственный медицинский университет» МЗ РФ, г. Краснодар;
Репс В.Ф., д.б.н., профессор, зав. отделом изучения механизмов действия физических факторов, ФГБУ «Пятигорский государственный НИИ курортологии» ФМБА России, г. Пятигорск.
Библиографическая ссылка
Шевченко А.М., Науменко А.Г., Благоразумная Н.В. РАЗРАБОТКА МЕТОДИК АНАЛИЗА ТАБЛЕТОК С СУХИМИ ЭКСТРАКТАМИ РАСТОРОПШИ, БЕССМЕРТНИКА И БИОМАССОЙ ГРИБА FUSARIUM SAMBUCINUM, ПОКРЫТЫХ ПЛЕНОЧНОЙ ОБОЛОЧКОЙ // Фундаментальные исследования. – 2015. – № 2-21. – С. 4699-4704;URL: https://fundamental-research.ru/ru/article/view?id=38053 (дата обращения: 26.04.2024).