Введение
Макрофаги играют исключительно важную роль в иммунных ответах. Это связано с тем, что внедрение в организм чужеродного агента вызывает прежде всего мощную активацию макрофагов, выделение цитокинов и других медиаторов воспаления. При этом в зависимости от микроокружения макрофаги могут существенно модифицировать свою активность. Так, макрофаги, находящиеся в среде с низкими дозами бактериального липополисахарида (ЛПС) и / или IFN-γ, в ответ на действие стимулирующих факторов отвечают классической активацией, т. е. продукцией провоспалительных цитокинов, таких, как IL-1, TNF-α, IL-12 и IFN-γ, и генерацией активных форм кислорода и азота. Такой фенотип макрофагов получил название M1 [8]. M1 макрофаги обладают выраженными фагоцитирующими и бактерицидными свойствами и уничтожают внутриклеточных микробов, таких, как вирусы и бактерии, а также опухолевые клетки. Макрофаги, находящиеся в среде с IL-4, IL-13, TGF-ß или глюкокортикоидами, формируют альтернативный М2 фенотип, который в ответ на действие стимулирующих факторов продуцирует антивоспалительные цитокины, такие, как IL-10, IL-13 [8]. M2 макрофаги уничтожают экстраклеточных паразитов, таких, как гельминты и грибы, содействуют ангиогенезу, репарации и ремоделированию тканей, но при этом могут способствовать опухолевому росту. Особая активация М2 фенотипа была обозначена новым термином «альтернативная активация» для подчеркивания контраста с «классической активацией» М1 макрофагов.
В очаге воспаления макрофаги функционируют в агрессивной среде, и для того чтобы выжить, макрофаги активируют синтез собственных внутриклеточных защитных стресс-белков HSP70 [7]. Индукция HSP70 представляет собой ключевой маркерный компонент так называемого стресс-ответа, который защищает макрофаги от некроза и апоптоза [7], индуцируемого различными воспалительными медиаторами. Таким образом, способность макрофагов к индукции HSP70, по сути, определяет, сможет ли макрофаг проявить свою иммунологическую активность в очаге воспаления. По сравнению с другими клетками макрофаги проявляют наибольшую способность активировать синтез HSP70 в ответ на действие провоспалительных цитокинов и компонентов бактериальных клеток, включая ЛПС [7].
Очевидно, что факторы, которые могут влиять на процесс формирования фенотипа макрофагов, на их секреторную активность и способность к индукции HSP70, представляют кардинальный интерес для современной иммунологии и медицины.
В качестве такого фактора, в настоящее время серьезное внимание привлекает сурфактантный белок D (SP-D). SP-D является мультимерным Са2+-связывающим белком из семейства коллагеноподобных лектинов. Главным образом, SP-D продуцируется в легких [5]. Недавно было показано, что в зависимости от своей олигомерной структуры SP-D может связываться или с CD91, или SIRP-α (сигнальный ингибирующий регуляторный белок-α) на поверхности альвеолярных макрофагах и соответственно стимулировать про- или антивоспалительную активность макрофагов [5]. Основная функция легочных SP-D состоит в модулировании воспаления и иммунной защиты в легких. Было показано, что удаление SP-D гена (SP-D (- / -)) приводит к увеличению количества и размера макрофагов в легких, нарушению профиля сурфактантных фосфолипидов, увеличению активности металлопротеаз, оксидативному и нитрозативному стрессу [9], а также повышению базального уровня воспаления в легких с последующим развитием эмфиземы [3] и повышению восприимчивости организма к бактериальным и вирусным инфекциям.
Недавно SP-D был обнаружен не только в легких, но и в сердце, желудке и кишечнике [4]. После этого сразу возник важный вопрос: может ли SP-D регулировать секреторную активность других макрофагов, кроме альвеолярных? То есть является ли SP-D только локальным фактором легочного иммунитета или он также может быть вовлечен в иммунный ответа всего организма. Недавно мы получили данные, которые позволили положительно ответить на этот вопрос, а именно: мы показали, что SP-D фенотип-зависимым образом влияет на продукцию NO и цитокинов перитонеальными макрофагами. При этом оказалось, что SP-D также играет роль и в самом процессе альтернативного программирования фенотипа макрофагов. Вместе с тем, вопрос о том, как влияет SP-D на способность макрофагов к индукции стресс-белков, и зависит ли это влияние от фенотипа макрофагов, до сих пор остается открытым.
Цель исследования
Цель работы состояла в том, чтобы определить, влияет ли SP-D на способность макрофагов к индукции стресс-белков HSP70, и если да, то является ли этот эффект фенотип-зависимым. Для того чтобы ответить на этот вопрос, мы сравнили степень ЛПС-индуцированного синтеза HSP70 в разных фенотипах перитонеальных макрофагов, выделенных от нормальных и SP-D (- / -) мышей.
Материал и методы исследования
C57BL / 6 мыши, не имеющие SP-D гена (SP-D (- / -)), были получены в лаборатории S. Hawgood и переданы в Пенсильванский университет США для дальнейших исследований. Сопоставимые по возрасту (8-10 недель) C57BL / 6 нормальные мыши были использованы в качестве контроля. Мыши содержались в условиях аккредитованного вивария, не допускающих попадание патогенных микроорганизмов, в соответствии с протоколом Комиссии по содержанию животных (Пенсильванский университет, США). Перитонеальные макрофаги выделяли из перитонеального смыва контрольных и SP-D (- / -) мышей, которым за 4 дня вводили в / б 2 мл 4 % бульона тиогликолята. Перитонеальные макрофаги культивировали в среде RPMI 1640 с 10 %-ной сывороткой с 100 U / мл пенициллина и 100 µг / мл стрептомицина в 48-ми луночных планшетах по 0,5x106 клеток на лунку. Для получения М1 и М2 фенотипов макрофагов была использована методика Zhang and Morrison [2]. Для этого первичная культура нативных перитонеальных макрофагов была разделена на три пула. В первый пул для формирования М1 фенотипа было добавлено на 6 часов 0,5 нг / мл ЛПС (из E. coli O111:B4, List Biologic Laboratories, Campbell, CA); во второй пул для формирования М2 фенотипа - 5 нг / мл ЛПС. Третий пул служил контролем (нативный М0 фенотип). Для активации макрофагов использовали ЛПС в концентрации 500 нг / мл.
Для подтверждения феномена репрограммирования макрофагов оценивали продукцию маркерного для М1 фенотипа интерлейкина 12 (IL-12); и маркерного для М2 фенотипа IL-10. Для измерения цитокинов 200 мкл культуральной среды замораживали при -800C. Оценку содержания IL-12 и IL-10 проводили с помощью SearchLight® Technology multiplex cytokine assay (Pierce Biotechnology, Woburn, MA). Результаты представляли как M + СО и обрабатывали статистически с использованием t-критерия Стьюдента. Отличие между группами считалось достоверным при p < 0,05.
Оценку содержания белка HSP70 проводили с помощью Вестерн-блот анализа. Для этой цели макрофаги лизировали в буфере, содержащем 62,5 мМ Tris-HCl, pH 6,8, 2 % SDS, 25 % глицерол, 0,01 % Bromophenol Blue. Белки электрофоретически разделяли с помощью SDS PAGE и электрофоретически переносили на PVDF мембрану (Bio-Rad) в присутствии 48 мМ Tris, 380 мМ глицина, 0,1 %SDS, 20 % метанола, pH 8,3. Неспецифическое связывание на мембране блокировали 5 % обезжиренным молоком в PBS-Tween в течение ночи при 4 ºC. Затем блоты инкубировали в течение 1 часа с первичными моноклональными мышиными анти-HSP70 антителами, которые распознают индуцибельные HSP70, при разведении 1:1000 (Stressgen, Cat # SPA-810). В качестве вторичных антител использовали конъюгированные с пероксидазой хрена антимышиные антитела (Santa Cruz, Cat # sc-2005) в разведении 1:3000. Просмотр бэндов осуществлялся с использованием хемилюминесценции (ECL+, Amersham Inc., Pittsburgh, PA), количественное определение проводилось путем денситометрического сканирования экспонированных пленок или направленным просмотром на устройстве Kodak 440 Imaging System (New Haven, CT). Измерение HSP70 проводили до и через 24 часа после активации макрофагов с помощью ЛПС (500 нг / мл). Способность к индукции HSP70 выражали в процентах как отношение содержания HSP70 через 24 часа стимуляции ЛПС к исходному уровню HSP70 до стимуляции, которое принимали за 100 %.
Результаты исследования и их обсуждение
Формирование М1 и М2 фенотипов макрофагов по методике Zhang и Morrison [2] мы подтвердили с помощью измерения цитокинов после стимуляции макрофагов ЛПС (рис. 1).
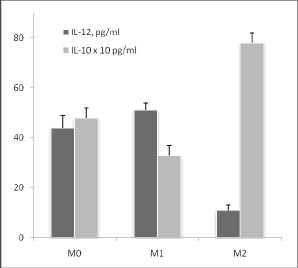
Рис. 1. Продукция IL-12 и IL-10 макрофагами М0, М1 и М2 фенотипа в ответ на действие 500 нг / мл ЛПС в течение 24 часов:
* - достоверность различий между М0 и М1 фенотипами
# - достоверность различий между М0 и М2 фенотипами
@ - достоверность различий между М1 и М2 фенотипами
Действительно, М1 макрофаги продуцировали преимущественно провоспалительный цитокин IL-12, а М2 - антивоспалительный IL-10. Эти данные принципиально не отличались от уже опубликованных ранее. На рис. 1 видно, что отсутствие гена SP-D привело к увеличению ЛПС-индуцированной продукции IL-12 в М1 фенотипе и не повлияло на продукцию этого фенотипа в М0 и М2 фенотипах. ЛПС-индуцированная продукция IL-10 была снижена в М0 и М2 фенотипах, и осталась неизменной в М1 фенотипе макрофагов SP-D (- / -) мышей по сравнению с нормальными макрофагами тех же фенотипов.
Данные, представленные на рис. 2, показывают, что все три фенотипа перитонеальных макрофагов нормальных мышей отвечали значительной активацией синтеза HSP70 на действие 500 нг / мл ЛПС.
Содержание HSP70 увеличивалось более чем в 100 раз. При этом оказалось, что предварительное репрограммирование макрофагов на М1 и М2 фенотипы практически не повлияло на способность нормальных макрофагов индуцировать синтез защитных стресс-белков. Наблюдалась лишь тенденция к снижению ЛПС-индуцированного синтеза HSP70 в М1 фенотипе по сравнению с М0 и М2 фенотипе по сравнению с М1.
В макрофагах SP-D (- / -) мышей в ответ на стимуляцию высокими концентрациями ЛПС (500 нг / мл) наблюдалась следующая картина (рис. 2). Удаление гена SP-D привело к тому, что ЛПС-индуцированный синтез HSP70 в нативном М0 фенотипе был незначительно выше, в М1 фенотипе практически не изменялся, а в М2 фенотипе был более чем в 2 раза увеличен по сравнению с соответствующим фенотипом макрофагов нормальных мышей. Эти данные отражают выраженную зависимость эффектов SP-D на синтез HSP70 от фенотипа перитонеальных макрофагов.
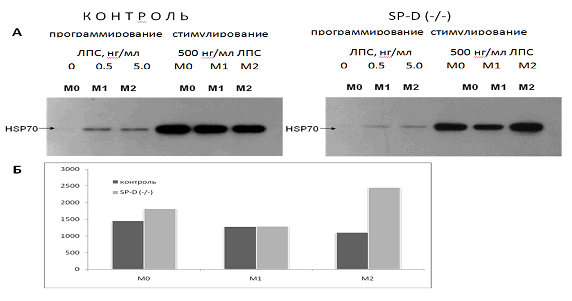
Рис. 2. Увеличение содержания HSP70 в макрофагах М0, М1 и М2 фенотипов в ответ на действие 500 нг / мл ЛПС в течение 24 часов. Макрофаги были выделены из перитонеальной жидкости нормальных (контроль) и SP-D (- / -) мышей:
А - репрезентативная фотография Вестерн блот анализа. Эксперимент проведен в трех повторах;
Б - графическое изображение данных Вестерн блот анализа (рис. 2 А) в процентах. За 100 % принято содержание HSP70 перед добавлением 500 нг / мл ЛПС
До 90-х годов исследования механизмов активации макрофагов фокусировались, главным образом, на индукции воспалительных и эффекторных функций. Открытие и описание М1 и М2 фенотипов макрофагов, вырабатывающих разный спектр Th1 и Th2 цитокинов, привело к разработке новой М1 / М2 концепции роли макрофагов в иммунитете. В этой концепции качество, интенсивность и специфичность активации макрофагов зависят от природы действующего патогена и модулирующих цитокинов [1]. Эти исследования обеспечили физиологическую основу для объяснения функциональной гетерогенности макрофагов, роли микроокружения в формировании фенотипа макрофагов и механизмов пластичности иммунного ответа. В этой работе мы сосредоточились на механизме индукции HSP70, который обеспечивает выживание макрофагов в неблагоприятной среде очага воспаления, и роли SP-D в регуляции этого защитного механизма.
Полученные нами результаты впервые показали, что SP-D вовлечен в регуляцию стресс-ответа макрофагов, и одновременно поставили два важных вопроса.
Первый вопрос, который возникает при анализе наших результатов - почему эффект удаления гена SP-D на синтез HSP70 зависит от фенотипа макрофагов. Очевидное предположение, что ЛПС-зависимое репрограмирование фенотипа макрофагов также «затрагивает» гипотетические пока механизмы SP-D-зависимого синтеза HSP70. На сегодняшний день у нас нет каких либо данных, которые помогли бы более конкретно интерпретировать этот результат.
Второй вопрос - почему удаление гена SP-D приводит к такому существенному увеличению индукции HSP70 в М2 фенотипе. Пока мы также не можем ответить на этот вопрос без дополнительных экспериментов. Вместе с тем увеличенный синтез HSP70 в М2 фенотипе макрофагов SP-D (- / -) мышей является четким указанием на то, что по крайне мере в М2 фенотипе макрофагальный SP-D играет негативную роль в отношении ЛПС-индуцированного стресс-ответа макрофагов. Действительно, хорошо доказано, что SP-D может ограничивать взаимодействие ЛПС со своим рецептором TLR4 (Toll-like receptor 4) на поверхности макрофагов и, таким образом, ингибировать ЛПС-зависимую активацию NFkB [10]. Можно было бы предположить, что в М2 фенотипе макрофагов SP-D (- / -) мышей резкое увеличение синтеза HSP70 в ответ на действие ЛПС связано с отсутствием негативного контроля SP-D и более эффективным связыванием ЛПС с TLR4. Недостающими звеньями этой гипотезы является отсутствие данных о том, что ЛПС-индуцированный синтез HSP70 вовлекает активацию NFkB.
Дополнительный намек на то, почему удаление гена SP-D приводит к такому существенному увеличению индукции HSP70 в М2 фенотипе, возникает при сопоставлении наших данных о влиянии удаления гена SP-D на продукцию цитокинов IL-12 и IL-10 с изменением синтеза HSP70 в разных фенотипах макрофагов (рис. 3).
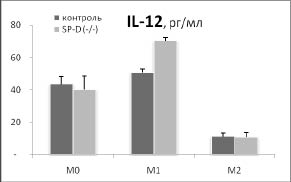
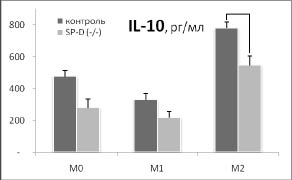
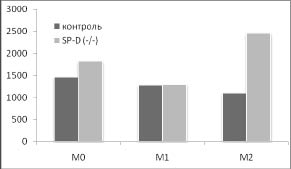
Рис. 3. Сопоставление влияния удаления гена SP-D на продукцию цитокинов и синтеза HSP70 в макрофагах М0, М1 и М2 фенотипов в ответ на действие 500 нг / мл ЛПС в течение 24 часов. Макрофаги были выделены из перитонеальной жидкости нормальных (контроль) и SP-D (- / -) мышей.
* - достоверность различий между контролем и SP-D (- / -).
Хорошо видно, что в отличие от IL-12, IL- 10 имеет четкую отрицательную корреляцию с изменением синтеза HSP70 в разных фенотипах при удалении гена SP-D. Можно предположить, что повышение синтеза HSP70 в М2 фенотипе макрофагов SP-D (- / -) мышей опосредовано снижением продукции IL-10. Это предположение поддерживают данные о том, что IL-10 действительно может угнетать индукцию HSP70 [6].
В целом наши данные еще раз подтверждают, что регуляторные эффекты SP-D зависят от фенотипа макрофагов, и свидетельствуют о важной роли SP-D в сопряжении и согласованной регуляции секреторной активности и клеточного стресс-ответа в макрофагах.
СПИСОК ЛИТЕРАТУРЫ
- Adams D. O., Hamilton T. A. Molecular basis of macrophage activation: diversity and its origins Lewis, C. E. McGee, J. O. eds. The Macrophage,1992, 75-114 Oxford University Press Oxford, UK.
- Atochina E., Beers M., Tomer Y. et al. Attenuated allergic airway hyperresponsiveness in C57BL / 6 mice is associated with enhanced surfactant protein (SP) -D production following allergic sensitization. Respir Res., 2003; 4: 15.
- Botas C., Poulain F., Akiyama J. et al. Altered surfactant homeostasis and alveolar type II cell morphology in mice lacking surfactant protein D. Proc.Natl.Acad. Sci. USA 95; 1998:11869-1187.
- Fisher J. H., Sheftelyevish V., Ho Y.-S. et al. Pulmonary-specific expression of SP-D corrects pulmonary lipid accumulation in SP-D gene-targeted mice. Am. J. Physiol. Lung Cell Mol. Physiol., 2000; 278: L365-L373.
- Guo C. J., Atochina-Vasserman E. N., Abramova H. et al. S-Nitrosylation of surfactant protein-D controls inflammatory function. PLoS Biology, 2004; 6 (11).
- Hoegl S., Boost K. A., Czerwonka H. et al. Inhaled IL-10 reduces biotrauma and mortality in a model of ventilator-induced lung injury. Respir Med., 2009; 103 (3): 463-70.
- Malyshev I. Yu., Kruglov S. V., Bakhtina L. Yu. et al. Stress response and apoptosis in pro- and antiinflammatory macrophages. Bulletin of Experimantal Biology and Medicine, 2004; 138 (8): 140-143.
- Martinez F. O., Sica A., Mantovani A. et al. Macrophage activation and polarization. Front Biosci., 2008; 13: 453-61.
- Wert S. E., Yoshida M., LeVine A. M. et al. Proceedings of the National Academy of Sciences of the United States of America 97, 2000: 5972-5977.
- Yamazoe M., Nishitani C., Takahashi M. et al. Pulmonary surfactant protein D inhibits lipopolysaccharide (LPS) -induced inflammatory cell responses by altering LPS binding to its receptors. J Biol Chem., 2008; 283 (51): 35878-88.
Библиографическая ссылка
Е. Н. Вассерман, Е. В. Абрамова, С. В. Круглов, С. В. Лямина, Ш. Л. Шимшелашвили, Ю. И. Малышев, М. Ф. Беарс, А. Д. Гоу, И. Ю. Малышев ОТСУТСТВИЕ ГЕНА SP-D ПРИВОДИТ К УСИЛЕНИЮ ЛПС-ИНДУЦИРОВАННОГО СИНТЕЗА HSP70 В М2, НО НЕ В М1 ФЕНОТИПЕ ПЕРИТОНЕАЛЬНЫХ МАКРОФАГОВ: ВОЗМОЖНАЯ РОЛЬ ИНТЕРЛЕЙКИНА- 10 // Фундаментальные исследования. – 2010. – № 6. – С. 19-27;URL: https://fundamental-research.ru/ru/article/view?id=8951 (дата обращения: 27.04.2024).



