Изотопы широко применяются для анализа различных химических систем [1,3]. Изотопные эффекты в металлоорганических соединениях отчетливо проявляются в колебательных спектрах. В электронных спектрах, кроме водорода [3], изотопные сдвиги выражены слабо и мало заметны. В то же время электронные спектры наиболее чувствительны к изменению ближайшего окружения молекул [4].
Целью настоящей работы является исследование спектров пропускания литиевых солей различного изотопного состава ди–2-этилгексилфосфорной кислоты (Д2ЭГФК) с различными органическими растворителями для применения в изотопном анализе.
Методика подготовки образцовдля снятия спектров
Ди–2-этилгексилфосфорная кислота (Д2ЭГФК) разбавлялась различными растворителями, после чего по реакции ионного обмена насыщалась изотопами из растворов 0.1 N хлористого лития, обогащенных до 96 % по литию-6 и до 98 % по литию-7. Протекание реакции ионного обмена контролировали по изменению РН раствора. Концентрация ионов в растворе, объёмное соотношение жидких фаз и другие условия выбирались так, чтобы получить идентичную концентрацию изотопических ионов в образцах ионита. В качестве растворителей выбраны растворители парафинового ряда (СnH2n + 2), кислородсодержащие (эфиры, спирты), трибутилфосфат, фенол и азотсодержащие (8-оксихинолин). При насыщении Д2ЭГФК солями лития обнаружено изменение изотопного состава по литию в фазе ионита относительно водной фазы. Для увеличения достоверности результатов исследовались спектры ионитов КУ-2 с различной степенью сшивки в Н- и калиевой форме.
Экспериментальные данные и их обсуждение
Электронные спектры органических соединений на основе Д2ЭГФК в сочетании с различными растворителями в различных изотопных формах получены на люминесцентной установке, изготовленной на базе спектрографа ИСП-1 с компьютерной обработкой спектров. Изотопный анализ лития проводили методом вторичной ионной масс-спектрометрии на установке МС-7201М, оснащенной монопольным масс-спектрометром [5]. В качестве зондирующего использован пучок ионов Аr+ c энергией 4 кэВ, плотностью тока ~0,01 мА/см2, площадь сечения пучка поверхностью ~2 мм2, с чувствительностью по литию ~5∙10–6 ат. %. Относительная ошибка измерения тока с детектора вторичных ионов (ВЭУ-2А) – не более 5 %. Раствор солей лития наносили на подложку из серебра. Для увеличения точности изотопного анализа измеряли фоновый сигнал подложки без лития. Затем на подложку наносили раствор ионов лития, экстрагированных 0,1 N соляной кислотой из Д2ЭГФК в литиевой форме после изотопного обмена. Раствор лития на подложке испаряли при комнатной температуре до получения сухого остатка. При реэкстракции лития из Д2ЭГФК возможен изотопный кинетический эффект. Поэтому для изучения влияния данного эффекта на подложку наносили Д2ЭГФК в литиевой форме, после чего проводили масс-спектрометрический анализ. В пределах погрешности результат тот же.
Пример спектра приведен на рисунке. Характерные длины волн и отношение экстинкций даны в таблице (представлена часть данных). Во всех спектрах наблюдается сдвиг максимума полосы пропускания при переходе от одного вида растворителя к другому в ряду (СnH2n + 2), RO, RN, где символом R обозначен радикал органической молекулы. Наблюдается сдвиг максимума полосы пропускания при изотопном замещении, что может найти объяснение в неявно выраженном электронно-колебательном характере спектров. Изменение спектра Д2ЭГФК в гептане от спектра Д2ЭГФК с 8-оксихинолином может быть объяснено отличающейся дополнительной связью Li…N по сравнению с Li…0. В случае 8-оксихинолина жидкий ионит Д2ЭГФК служит растворителем. В частности, в спектре с изотопом Li7 наблюдаются два характерных максимума при 488,2 и 502,1 нм, а изотопный сдвиг Δλ для каждого из максимумов составляет около 10 нм. Для всех спектров характерно уменьшение интенсивности полос при замене лёгкого изотопа на тяжёлый (см. таблицу). Заметим, что, если освещать образцы Д2ЭГФК с легким и тяжелым ионами лазерным лучом (использовали две волны λ = 532 и 467 нм), сдвиг в спектрах настолько заметен визуально, что во всех 24 исследованных образцах безошибочно определяли тип изотопа, находящегося в фазе ионита.
Отношение экстинкций изотопных форм лития в соединениях Д2ЭГФК с растворителями и изотопический сдвиг в спектрах пропускания
|
Длина волны, нм |
Отношение экстинкций Li6/Li7 |
Растворитель |
Изотопический сдвиг Δλ, нм |
|
488 |
1, 2695 |
8-оксихинолин |
10,0 |
|
502 |
1,1933 |
8-оксихинолин |
10,1 |
|
471 |
1,2680 |
трибутилфосфат |
8,1 |
|
457 |
1,2522 |
гептиловый спирт |
6,1 |
|
463 |
1,1732 |
гептиловый эфир |
5,3 |
|
480 |
1,2432 |
фенол |
2,2 |
|
460 |
1,0565 |
без растворителя |
2,1 |
|
471 |
1,1440 |
КУ-2 |
5,4 |
Различие в массах двух изотопов мало, поэтому для более достоверной идентификации снят спектр жидкого ионита, насыщенного ионами калия (рисунок, кривая К). Этот спектр подтверждает зависимость положения максимума полосы пропускания от массы исследуемого иона. Спектры Д2ЭГФК + гептиловый спирт и Д2ЭГФК + гептиловый эфир аналогичны. Если спектр жидкого ионита с тяжёлым изотопом имеет равновероятные максимумы в области 450–480 нм, то спектр Д28ГФК с лёгким изотопом отличается наличием одного максимума при λ = 460 нм. В случае фенола характерен максимум для лёгкого изотопного иона при длине волны, равной 480 нм. Появление различий в максимумах спектров Д2ЭГФК с трибутилфосфатом, фенолом, гептиловым спиртом для изотопических ионов говорит о возможном перераспределении колебательной энергии в молекулах с разными изотопами или эффектом гидратации ионов лития. Для сравнения исследовали спектры гранулированного ионита КУ–2 и КУ-2-8 (тип Dowex– полистиролдивинилбензосульфонатная смола различной сшитости) в Н– и Li изотопных формах. За небольшим исключением их спектры практически идентичны. Это, вероятнее всего, можно объяснить тем, что в фазе гранулированного ионита вследствие его набухания ионы сильно гидратированы (т.е. сохраняют водную оболочку), а, следовательно, различие в массах ионов менее заметно.
При приготовлении образцов измеряли изотопный состав лития в фазе ионита. Однократный коэффициент разделения изотопов определяли как отношение концентраций изотопов в фазе ионита к отношению концентраций изотопов в фазе раствора [6, 7]. Его величина оказалась равной 1.008. Возможно, что эффект связан с доминированием стадии дегидратации при переходе катиона из водного раствора в фазу ионита. Этот вывод подтверждается квантовостатистическими расчетами [5, 8]. Например, известно, что иониты КУ-2 и его разновидности сильно набухают в воде. А увеличение степени сшивки приводит к уменьшению гидратации ионов лития и, как следствие, к увеличению КРИ с 1,008 до 1,012 [7]. В ряде экспериментов кювету с Д2ЭГФК и КУ-2 в Li-форме и водным раствором изотопов лития освещали через линзу-расширитель лазером KLM-457-x с длиной волны 457 нм, близкой к максимуму спектра Д2ЭКФК (см. таблицу). При воздействии лазерным излучением КРИ для КУ-2 увеличивается и достигает 1,012. В этих же условиях для ионита Д2ЭГФК КРИ возрастает с 1.006 до 1,014. Погрешность измерения составляет ±0,001. Этот результат, по-видимому, объясняется уменьшением числа молекул в гидратной оболочке аквакомплекса лития под действием лазерного облучения. В частности, уменьшение числа молекул воды в гидратной оболочке катионов при воздействии на растворы переменным электрическим полем отмечено в [2].
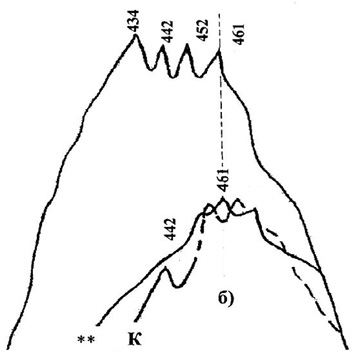
Пример спектров пропускания Д2ЭГФК (растворитель трибутилфосфат) в изотопной форме: верхний спектр – легкий изотоп лития, ** – тяжелый изотоп лития, К – Д2ЭГФК в калиевой форме (пунктир)
Заключение
Исследован изотопный сдвиг в спектрах пропускания литиевых соединений ди–2-этилгексилфосфорной кислоты (Д2ЭГФК) с различными органическими растворителями. Величина изотопного сдвига зависит от используемых растворителей и от изотопного состава лития в фазе Д2ЭГФК. Изотопный эффект в спектрах выражается в смещении на 10–12 нм в коротковолновую часть максимумов спектра при замене изотопов в фазе Д2ЭГФК. Насыщение Д2ЭГФК литиевыми солями сопровождается эффектом разделения изотопов лития. Эффект разделения увеличивается при лазерном облучении реакционной кюветы, где протекает реакция насыщения образцов изотопами. В целом исследованные спектры Д2ЭКФК можно использовать в аналитических целях, в частности проводить изотопный экспресс-анализ.
Рецензенты:
Пичугин В.Ф., д.ф.-м.н., профессор, заведующий кафедрой теоретической и экспериментальной физики, ФГБОУ ВПО «Национальный исследовательский Томский политехнический университет», г. Томск;
Арефев К.П., д.ф.-м.н., профессор, заведующий кафедрой высшей математики, ФГБОУ ВПО «Национальный исследовательский Томский политехнический университет», г. Томск.
Работа поступила в редакцию 16.04.2013.



