Шишковидная железа принимает участие в адаптации организма к различным видам стресса [9]. Морфологическими маркёрами сдвигов её функционального состояния рассматриваются изменения ядер и органелл в цитоплазме пинеалоцитов с секреторными везикулами и синаптическими лентами и сферами в цитоплазме, ранее называемых светлыми [10, 11, 12]. Светлые пинеалоциты секретируют хронобиотик гормон мелатонин преимущественно в тёмное время суток под контролем циркадианного пейсмекера – супрахиазматических ядер гипоталамуса. Ранее нами было выявлено, что у крыс при нарушении суточного фотопериодизма через 24 ч после окончания воздействия светом супрахиазматические ядра гипоталамуса и шишковидная железа реагируют на стресс [2, 9]. В шишковидной железе гипериллюминированных крыс в светлое время суток выявлялся мелатонин [1]. В пинеалоцитах увеличивались размеры ядрышек, ядра, складчатость его оболочки [7]. В цитоплазме клеток возрастал удельный объём митохондрий, комплекса Гольджи и гранулярной эндоплазматической сети. Комплекс Гольджи смещался от ядра на периферию перикарионов. Удлинялись синаптические ленты [8]. На 45-е и 90-е сутки освещения крыс диктиосомы в пинеалоцитах располагались вблизи ядра. Удельный объём комплекса Гольджи, митохондрий и размер ядер уменьшались [3]. При постоянной 12-часовой суточной фотофазе у крыс кариометрические параметры супрахиазматических нейронов
и пинеалоцитов проявляли инфрадианный ритм изменений в течение месяца [6]. При естественном укорочении суточной фотофазы у полёвок отмечались морфологические признаки активизации деятельности шишковидной железы [4]. Предполагается, что в секреторном процессе шишковидной железы у грызунов, наряду с митохондриями, комплексом Гольджи, цитоскелетом, синаптическими лентами и сферами, принимают участие осмиофильные тельца и везикулы с конкрециями [5]. Поскольку механизм секреции пинеалоцитов до настоящего времени остаётся невыясненным, интерес представляет исследование всего комплекса ультраструктур цитоплазмы, проявляющего себя при активизации их деятельности у различных видов грызунов в условиях стресса.
Цель настоящего исследования – изучение особенностей ультраструктуры пинеалоцитов с признаками функциональной активности в шишковидной железе крыс и полёвок в условиях стресса.
Материал и методы исследования
Исследование выполнено на самцах 4-месячных беспородных белых крыс (n = 12) и 2-месячных красно-серых полёвок (n = 11). Крыс содержали в условиях 12-часовой суточной фотофазы (свет с 8 до 20 ч, освещённость животных 200 лк). Группу опытных животных на 48 ч помещали в гипериллюминированные клетки (освещённость 3500 лк) и выводили из эксперимента через 24 ч после окончания воздействия совместно с контролем. Полёвок, рождённых в июле от изъятых из природной среды самок, содержали в естественных условиях освещения изолированно в выводке с матерями (контрольная группа) и совместно (опытная группа). Шишковидную железу извлекали в 10–11 ч после декапитации животных, фиксировали в 4 % параформальдегиде и 2,5 % глютаральдегиде на 0,1 М какодилатном буфере (рН 7,4), постфиксировали в 1 % растворе тетраоксида осмия, обезвоживали в этаноле и заключали в смесь смол эпон–аралдит. Срезы готовили на ультратоме «LКВ-III» (Швеция) и «Leica EM UC 7» (Австрия), контрастировали уранилацетатом и цитратом свинца, исследовали в электронном микроскопе JEM-100 СХ II («JEOL», Япония). При конечном увеличении 25000, используя программное обеспечение «Axio Vision 4.8.2» («Carl Zeiss», Германия), в пинеалоцитах измеряли площадь среза митохондрий. Данные обрабатывали с помощью пакета прикладных программ «Statistica for Windows v 6.0». О значимости различий судили по величине U-критерия Манна – Уитни. Данные представляли в виде медианы (Ме), верхнего и нижнего квартилей (Q1–Q2).
Результаты исследования
и их обсуждение
В светлых пинеалоцитах шишковидной железы у крыс и полёвок, подвергнутых различным видам стресса, обнаруживаются извитые и ковшеобразные митохондрии, площадь продольного среза которых в 1,3 раза превосходит величину показателя в контроле (таблица).
Площадь продольного среза митохондрий в пинеалоцитах у грызунов (Ме (Q1–Q2), мкм2)
|
Крысы |
Полёвки |
||
|
гипериллюминированные |
контроль |
совместное содержание |
контроль |
|
0,452* (0,429–0,465) |
0,354 (0,337–0,378) |
0,263* (0,253–0,274) |
0,205 (0,196–0,214) |
Примечание. * – значимые различия с контролем (р ≤ 0,05).
У крыс между завитками митохондрий располагаются микротрубочки и микрофиламенты, ориентированные веерообразно, секреторные везикулы с электронно-плотной сердцевиной, окружённой светлым ободком, цистерны и осмиофильные тельца с электронно-плотными гранулами, синаптические ленты. От поверхности пинеалоцитов в перикапиллярное пространство вблизи фенестрированных участков эндотелия отпочковываются мембранные структуры, опустошённые или ещё содержащие электронно-плотную гранулу в светлом матриксе (рис. 1). Подобные комплексы формируются также в местах контакта светлых пинеалоцитов друг с другом. Синаптические ленты, митохондрии, секреторные везикулы и цистерны гладкой эндоплазматической сети сближаются в контактирующих клетках с диктиосомами (рис. 2). У полёвок совместного проживания ковшеобразные митохондрии извитой «ручкой» и расширенной частью «зачерпывают» участки цитоплазмы с гранулярными секреторными везикулами, контактируют с цистернами гладкого эндоплазматического ретикулума. Веерообразно ориентированные микротрубочки и микрофиламенты объединяют митохондрии в единый комплекс с синаптическими сферами, секреторными везикулами, производными комплекса Гольджи и фрагментами цистерн гранулярной эндоплазматической сети, теряющими рибосомы (рис. 3).
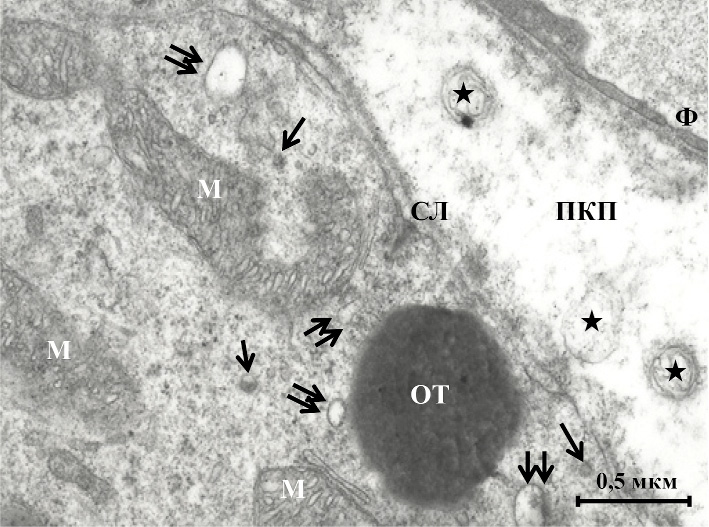
Рис. 1. Комплекс ультраструктур в цитоплазме
светлого пинеалоцита гипериллюминированной крысы:
М – митохондрии извитой формы, СЛ – синаптическая лента, ОТ – осмиофильное тельце. Секреторные везикулы обозначены стрелками, цистерны – двойными стрелками, мембранные структуры перикапиллярного пространства (ПКП) – звёздочками, Ф – фенестра
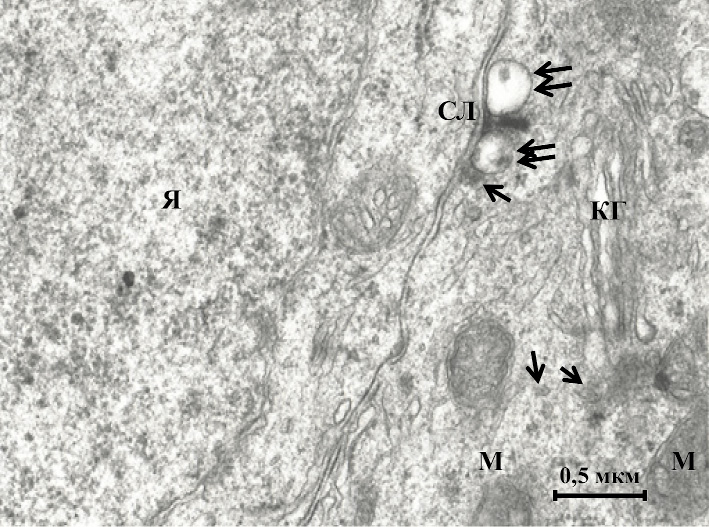
Рис. 2. Митохондрии, синаптическая лента, цистерны и секреторные везикулы
в пинеалоците гипериллюминированной крысы:
КГ – комплекс Гольджи, Я – ядро соседнего пинеалоцита, другие обозначения те же
Крупные размеры, извитая и выпукло-вогнутая форма, по-видимому, делает более эффективным взаимодействие митохондрий с окружающими структурами цитоплазмы пинеалоцитов при стрессе. Известно, что митохондрии не только обеспечивают энергией процессы синтеза веществ, двигательную активность компонентов цитоскелета, но и участвуют в обмене кальция, возможно, в наполнении цистерн гладкой эндоплазматической сети и осмиофильных телец кальцием с отложением конкреций. Везикулы с электронно-плотной гранулой, производные комплекса Гольджи, и осмиофильные тельца с вкраплениями электронно-плотных конкреций, производные комплекса Гольджи, лизосом и эндоплазматического ретикулума, в свою очередь, возможно, благодаря смещению песчинок, оказывают влияние на цитоскелет, опосредованный клеточными мембранами транспорт веществ, формирование синаптических лент и сфер. Увеличение числа синаптических лент и сфер в месте контакта пинеалоцитов с капиллярами и друг с другом при активизации деятельности шишковидной железы делает обоснованным предположение об их участии в механизме секреции и синхронизации функциональной активности клеток [12]. По данным литературы [10], митохондрии, кроме того, могут быть задействованы в обмене индоламинов. Индоламин мелатонин способен проникать через клеточные мембраны, связываться с белком-носителем в секреторных везикулах, производных комплекса Гольджи. Секреция сопровождается вытеснением кальцием мелатонина из комплекса с белком-носителем, отложением мозгового песка в перикапиллярном пространстве и включением мелатонина в кровоток. Не исключено, что структуры с конкрециями – везикулы и осмиофильные тельца также задействованы в транспорте и секреции мелатонина, отложении мозгового песка. Мерокринная нейросекреция, высвобождение через поры в плазмолемме содержимого секреторных везикул с электронно-плотной сердцевиной, окружённой светлым ободком, производных комплекса Гольджи, не является единственным механизмом, проявляющимся в шишковидной железе у грызунов при различных
видах стресса.
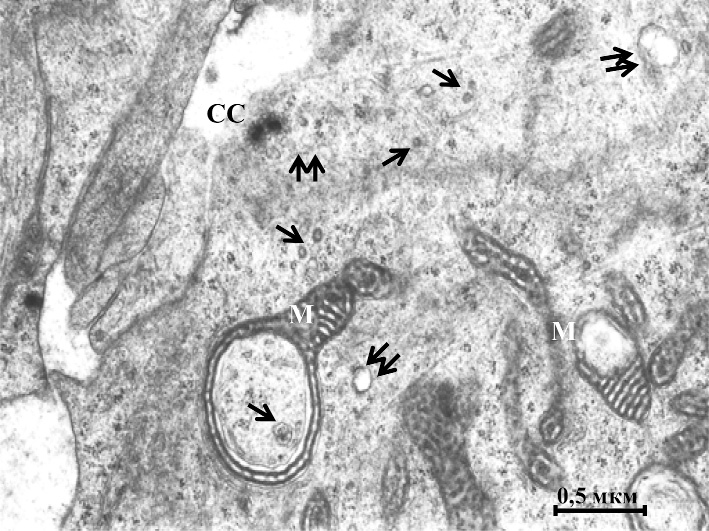
Рис. 3. Ковшеобразные митохондрии, секреторные везикулы и цистерны
в пинеалоците у полёвки совместного содержания:
СС – синаптические сферы, другие обозначения те же
Наличие мембранных структур с электронно-плотным материалом в перикапиллярном пространстве и теряющих рибосомы фрагментов цистерн гранулярного эндоплазматического ретикулума в перикарионах пинеалоцитов свидетельствует об апокринной эпендимоподобном характере секреции, при которой также, как и при механизме, подобном нейросекреции, организуются характерные комплексы митохондрий, синаптических лент и сфер, везикул, цистерн и осмиофильных телец с конкрециями.
Заключение
Проведённое морфологическое исследование даёт основание рассматривать комплексы, состоящие из удалённых от ядра стопок Гольджи, цистерн и осмиофильных телец с зёрнами электронно-плотного материала, гигантских извитых и ковшеобразных митохондрий, синаптических лент и сфер, гранулярных секреторных везикул и компонентов цитоскелета морфологическими маркёрами секреторной активности пинеалоцитов у грызунов при различных видах стресса.
Рецензенты:
Солонский А.В., д.м.н., ведущий научный сотрудник лаборатории клинической психонейроиммунологии и нейробиологии, ФГБУ «Научно-исследовательский институт психического здоровья» СО РАМН,
г. Томск;
Мустафина Л.Р., д.м.н., заведующая лабораторией кафедры гистологии, эмбриологии и цитологии, ГБОУ ВПО «Сибирский государственный медицинский университет» Министерства здравоохранения РФ,
г. Томск.
Работа поступила в редакцию 24.10.2014.



