Вирусы гриппа типа А являются высококонтагиозными респираторными патогенами, представляющими постоянную угрозу мировому сообществу. Ежегодные эпидемии гриппа вызывают от 3 до 5 миллионов случаев тяжелых респираторных заболеваний, не менее 250 тысяч из которых заканчиваются летальным исходом. Наиболее эффективным средством борьбы с гриппом является вакцинация. В настоящее время в практике здравоохранения применяется два вида гриппозных вакцин – инактивированные (ИГВ) и живые холодоадаптированные реассортантные (ЖГВ).
Иммунизация при помощи ИГВ приводит к формированию мощного гуморального иммунного ответа к поверхностным антигенам вируса гриппа – гемагглютинину (HA) и нейраминидазе (NA). Однако такой иммунный ответ является узкоспецифичным, т.е. неспособным защитить привитого от дрейфовых вариантов вируса гриппа. В отличие от ИГВ, иммунизация ЖГВ приводит к формированию широкого спектра иммунитета, включая индукцию местного (локального) иммунного ответа, а также стимуляцию CD8+ цитотоксических Т-лимфоцитов (ЦТЛ) [11]. Иммунитет, опосредованный ЦТЛ, является перекрестным к различным сероподтипам вируса гриппа А, поскольку эти клетки распознают консервативные участки вирусных белков. Таким образом обеспечивается перекрестная защита привитых от дрейфовых и даже пандемических вариантов вирусов гриппа А [9]. Основной мишенью для образования CD8+ Т-клеток является молекула нуклеопротеина вируса гриппа А, содержащая наибольшее число эпитопов для ЦТЛ [7].
Вакцинные штаммы для ЖГВ готовятся путем реассортации генов дикого циркулирующего вируса гриппа А и холодоадаптированного донора аттенуации
А/Ленинград/134/17/57 (H2N2). В результате вакцинный штамм приобретает гены поверхностных белков (HA и NA) от дикого вируса, а вся часть генов внутренних белков, в том числе нуклеопротеина (NP) – от донора аттенуации [1]. Последние определяют безвредность (аттенуацию) ЖГВ. Однако донор аттенуации был получен из штамма 1957 года выделения и за более чем 50 лет нуклеопротеин циркулирующих вирусов мог значительно эволюционировать. Это несоответствие могло отразиться на антигенных свойствах современных вирусов и, как следствие, снижать спектр эффективности цитотоксического иммунитета у людей при вакцинации вирусом с антигенно устаревшим геном NP.
Цитотоксические T-клетки распознают пептиды, представленные молекулами МНС с помощью Т-клеточного рецептора. Презентация вирусных пептидов в составе молекул МНС класса I обеспечивает элиминацию инфицированных клеток цитотоксическими CD8+ Т-клетками. Эффективность презентации вирусного пептида (способности быть эпитопом) складывается из двух составляющих: процессинга пептидов в пути презентации с МНС молекулами I класса и иммуногенности комплекса пептид-МНС. Основанные на анализе процессинга и презентации пептидов математические модели предсказания иммунодоминантных эпитопов недавно стали доступны в базе данных The immune epitope database 3.0 (IEDB) [14].
Целью настоящего исследования явился сравнительный анализ in silico молекулярной эволюции ЦТЛ-иммуноэпитопов нуклепротеина современных циркулирующих вирусов гриппа А (H1N1 и H3N2) в сравнении с донором аттенуации А/Ленинград/134/17/57 (H2N2) – Лен/17.
Материалы и методы исследования
Алгоритм настоящего исследования приведен на рисунке. Анализ данных проводился в несколько этапов, описание которых приведено ниже.
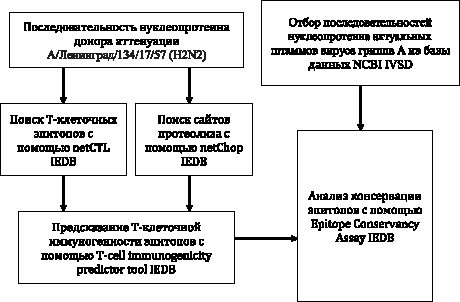
Алгоритм проведения in silico анализа консервации (консервативности) иммунногенных Т-клеточных МНС-I эпитопов нуклеопротеина в актуальных циркулирующих штаммах вируса гриппа А. NCBI IVSD – NCBI Influenza Virus Sequence Database, IEDB – The immune epitope database
Отбор последовательностей нуклеопротеина актуальных штаммов вируса гриппа А проводили с помощью базы данных NCBI Influenza Virus Sequence Database [2]. Отбирали уникальные полные белковые последовательности нуклеопротеина вируса гриппа А подтипов H1N1 и H3N2, выделенных повсеместно от человека с 2009 года по настоящее время (октябрь 2014). Из поиска были исключены лабораторные штаммы. После выравнивания алгоритмом CrustalO [13] и проверки на отсутствие полной гомологии было получено 757 уникальных последовательностей (табл. 1). Последовательность нуклеопротеина Лен/17 была получена из локальной базы данных отдела вирусологии им. А.А. Смородинцева, ФГБУ НИИЭМ СЗО РАМН [8]
Таблица 1
Объем выборки изолятов вируса гриппа А в проводимом исследовании
|
Год выделения |
Количество исследуемых нуклеопротеиновых последовательностей вирусов гриппа А серотипов |
|
|
H1N1 |
N3N2 |
|
|
2009 |
367 |
57 |
|
2010 |
65 |
37 |
|
2011 |
44 |
39 |
|
2012 |
10 |
40 |
|
2013 |
31 |
46 |
|
2014 |
20 |
1 |
Поиск Т-клеточных эпитопов проводили в базе данных иммунноэпитопов IEDB с помощью алгоритма предсказания ЦТЛ-эпитопов netCTL [10]. Параметры вклада С-концевого протеолиза, эффективности транспорта TAP (Transporter associated with antigen processing), порога отбора эпитопов были 0,15; 0,05 и 0,75, соответственно. Картирование эпитопов на последовательности вакцинного штамма вируса гриппа А Лен/17 производилось с помощью алгоритма выравнивания CrustalO в программе Jalview 2.8.1.
Предсказание Т-клеточной иммуногенности эпитопов проводили в базе данных иммуноэпитопов IEDB с помощью алгоритма T cell class I pMHC immunogenicity predictor [5]. Маскирование пептидов было проведено по 1, 2 и С-концевой аминокислотам. Эпитопы с баллом иммуногенности больше 0 (средний балл для неиммуногенных пептидов [5]) были отобраны для дальнейшего анализа
Поиск сайтов протеолиза нуклеопротеина проводили в базе данных иммунноэпитопов IEDB с помощью алгоритма протеосомного процессинга пептидов netChop [12]. Использовали метод анализа С-концевого протеолиза 3.0 с порогом 0,5.
Анализ консервации эпитопов проводили в базе данных иммуноэпитопов The immune epitope database (IEDB) 3.0 с помощью алгоритма epitope Conservancy Analysis [4] в режиме оценки линейных эпитопов с порогом идентичности последовательности не менее 100 %. Идентичные последовательности удалялись перед анализом. Консервация эпитопа выражалась в виде процента штаммов с полностью гомологичными ему последовательностями относительно всей исследуемой выборки вирусов гриппа А.
Результаты исследования
и их обсуждение
При поиске Т-клеточных эпитопов в последовательности нуклеопротеина вируса гриппа Лен/17 было выявлено 210 9-мерных эпитопов для двенадцати HLA супертипов класса I (А1, А2, А3, А24, А26, B8, B27, B39, B44, B58, B62). Около половины эпитопов (103/210) были уникальными и связывались с молекулами HLA не более одного супертипа. После объединения общих эпитопов для нескольких HLA-супертипов были получены 138 уникальных последовательностей. Далее список из 138 эпитопов был ограничен теми, которые проходили проверку теста предсказания иммуногенности Т-клеточных эпитопов. Доля иммуногенных эпитопов составила 49 % (68/138). Для исключения эпитопов с высоким риском протеолиза при протеосомном процессинге нуклеопротеина, из 68 были отобраны эпитопы не более чем с 1 предсказанным сайтом протеолиза. Доля эпитопов нуклепротеина Лен/17, прошедших эту проверку, составила 26 % (18/68). Таким образом, с помощью применённого алгоритма (рисунок) были отобраны 18 из 210 проанализированных эпитопов, которые отвечали критериям ЦТЛ-иммуногенности и малой вероятностью протеолиза.
В табл. 2 представлены результаты анализа консервации иммуногенных эпитопов Лен/17. Анализ консервации позволяет оценить долю вирусов из исследуемой выборки, несущих в нуклеопротеине полностью гомологичные Лен/17 эпитопы (далее процент консервации). Из данных табл. 2 видно, что лишь 8 из 18 отобранных эпитопов (44,4 %) были высококонсервативны, т.е. сохранялись в большинстве исследуемых нуклепротеинов вируса гриппа А (90 % и более штаммов с идентичными последовательностями). Тогда как остальные 10 иммуногенных эпитопов были идентичны лишь у 4–33 % современных циркулирующих вирусов гриппа А. Такая вариация в степени консервативности этих эпитопов говорит о различных механизмах селектирующего действия на вирусы. Опираясь на полученные данные, можно говорить о двух типах отбора иммуногенных ЦТЛ-эпитопов. В первую группу эпитопов входят высококонсерватиные последовательности (с процентом консервации более 90 %), во-вторую – низкоконсервативные последовательности (с консервацией 4–33 %). Оценка влияния отбора на эпитопы требует проверки и может быть установлена с помощью алгоритмов оценки молекулярной эволюции [6].
Таблица 2
Консервативность ЦТЛ-эпитопов нуклеопротеина (NP) донора
аттенуации А/Ленинград/134/17/57 (H2N2) по отношению к современным штаммам вирусов гриппа А (H1N1 и H3N2)
|
Эпитопы NP вируса гриппа А/Ленинград/134/17/57 (H2N2) |
Консервация Т-клеточных эпитопов NP в штаммах вируса гриппа А 2009–2014 гг., % |
Предсказание Т-клеточной иммуногенности эпитопа, баллы |
Количество вероятных сайтов протеолиза |
|||
|
Номер эпитопа |
Позиция на транскрипте NP |
Связывающий эпитоп HLA-супертип |
Аминокислотная последовательность |
|||
|
84, 136 |
198–206 |
A24, B27 |
KRGINDRNF |
98,6 % |
0,20 |
1 |
|
177 |
199–207 |
B58 |
RGINDRNFW |
98,6 % |
0,17 |
1 |
|
31 |
200–208 |
A3 |
GINDRNFWR |
98,4 % |
0,29 |
1 |
|
141 |
174–182 |
B27 |
RRSGAAGAA |
98,4 % |
0,11 |
1 |
|
38 |
317–325 |
A3 |
RPNENPAHK |
97,9 % |
0,13 |
1 |
|
138, 142 |
245–253 |
B27, B39 |
SRNPGNAEI |
97,8 % |
0,11 |
1 |
|
52 |
66–74 |
A3 |
MVLSAFDER |
97,4 % |
0,06 |
1 |
|
11 |
250–258 |
A1 |
NAEIEDLIF |
92,9 % |
0,35 |
1 |
|
167 |
114–122 |
B44 |
EEIRRIWRQ |
33,0 % |
0,49 |
1 |
|
50, 165 |
23–31 |
A3, B44 |
TEIRASVGK |
27,7 % |
0,03 |
1 |
|
100 |
439–447 |
A26 |
DMRAEIIRM |
27,6 % |
0,42 |
0 |
|
51 |
438–446 |
A3 |
SDMRAEIIR |
27,6 % |
0,32 |
1 |
|
49 |
30–38 |
A3 |
GKMIDGIGR |
27,0 % |
0,26 |
1 |
|
119 |
276–284 |
B8 |
LPACVYGPA |
5,8 % |
0,02 |
1 |
|
159 |
17–25 |
B44 |
GERQNATEI |
4,9 % |
0,02 |
1 |
|
145 |
125–133 |
B39 |
NGDDATAGL |
4,4 % |
0,16 |
1 |
|
89, 206 |
211–219 |
A26, B62 |
NGRKTRIAY |
4,2 % |
0,02 |
1 |
|
134 |
213–221 |
B27 |
RKTRIAYER |
4,0 % |
0,29 |
1 |
Более того, в штаммах с отсутствием полностью гомологичных исследуемым эпитопам последовательностей совпадало от 5 до 8 аминокислотных остатков в 9-мерных пептидах. Замена даже одной аминокислоты может кардинально изменять иммуногенность пептида [3].
Важно отметить, что из семи наиболее иммуногенных эпитопов нуклеопротеина вируса Лен/17 (с уровнем предсказанной иммуногенности выше 0,2) лишь два эпитопа (NP250-258 и NP200-208) встречались у большинства циркулирующих штаммов вируса гриппа А (92–98 %). Остальные 5 иммуногенных эпитопов нуклеопротеина Лен/17 (114–122, 439–447, 438–446, 213–221 и 30–38) встречались только у 4–33 % современных вирусов.
Эти данные свидетельствуют о том, что ЦТЛ иммунный ответ, индуцированный вакцинацией штаммами ЖГВ, содержащими ген NP от вируса Лен/17, может быть направлен на 8 из 18 эпитопов (или на 2 из 7 высокоиммуногенных эпитопов) против инфекции актуальными вирусами гриппа А, что может сказаться на выраженности и спектре действия вирус-специфичного ЦТЛ иммунитета.
Устранить указанный недостаток современных штаммов ЖГВ можно двумя способами: первое – переносить в геном вакцинных штаммов ЖГВ, помимо поверхностных антигенов современных циркулирующих вирусов гриппа А, также и их NP ген. Второе – выявить аминокислотные остатки в NP белке донора аттенуации Лен/17, отличающиеся от циркулирующих штаммов вируса гриппа А и находящиеся в иммунодоминантных ЦТЛ-эпитопах последних. Точечный мутагенез таких аминокислот с помощью методов обратной генетики позволит создавать вакцинные штаммы ЖГВ с актуальным набором иммунодоминантных эпитопов в их нуклеопротеине.
Заключение
С помощью математических моделей было предсказано наличие иммуногенных Т-клеточных эпитопов в нуклеопротеине донора аттенуации А/Ленинград/134/17/57 (H2N2), презентируемых в составе молекул МНС класса I. При анализе консервации показано, что больше половины этих эпитопов отсутствует у подавляющего числа современных вирусов гриппа А подтипов H1N1 и H3N2, циркулирующих с 2009 года. Эти данные свидетельствуют о возможном недостаточно широком спектре цитотоксических вирус-специфичных Т-клеток индуцированных ЖГВ для защиты от актуальных
вирусов гриппа А. Обнаруженные эпитопы могут быть использованы в качестве перспективных мишеней для создания обратно-генетических вакцининдуцирующих широкий перекрестный цитотоксический Т-клеточный иммунитет против актуальных штаммов на основе донора аттенуации А/Ленинград/134/17/57.
Исследование выполнено при финансовой поддержке гранта Российского Научного Фонда № 14-15-00034.
Рецензенты:Назаров П.Г., д.м.н., профессор, зав. отделом иммунологии, ФГБУ «НИИЭМ» СЗО РАМН, г. Санкт-Петербург;
Кривицкая В.З., д.б.н., ведущий научный сотрудник лаборатории биотехнологии диагностических препаратов отдела биотехнологии, ФГБУ «НИИ гриппа» МЗ РФ, г. Санкт-Петербург.



