Развитие современной техники требует разработки новых и совершенствования имеющихся способов получения материалов с высокими эксплуатационными характеристиками. К числу таких материалов относятся оксидные шпинели. Перспективным объектом исследования для получения материалов с необычными свойствами, востребованными в различных прикладных областях, в частности химической промышленности, космической технике, является шпинель состава Fe2TiO4 [9]. Известно, что композиционные материалы, содержащие соединения титана, отличаются высокой каталитической активностью [6, 7], при этом проявляют супермагнитные свойства [7]. Теоретические основы формирования структуры подобных соединений были рассмотрены ранее [1, 8]. Фундаментальный научный интерес к изучению процессов фазообразования и свойств подобных материалов обусловлен в первую очередь их уникальным катионным составом и сложностью получения материалов, содержащих ионы Fe2+ и Ti4+. Для синтеза подобных соединений используют специальную аппаратуру [9], способную обеспечить проведение реакции в контролируемой (чаще всего – инертной) атмосфере. Как правило, в окислительной атмосфере затруднен процесс получения соединения, содержащего Fe2+ [4]. Для стабилизации данного валентного состояния катиона железа было предложено [4] использовать в качестве матрицы формирующийся твердый раствор со структурой шпинели. В этой связи разработка методики синтеза, изучение фазообразования и свойств в системе TiO2 – FeO – Fe2O3 представляет фундаментальный и практический интерес для химии и технологии неорганических материалов. Целью исследования являлось изучение процессов формирования структуры в системе TiO2/Fe1,92Ti0,61O4/Fe2O3 и ее каталитических свойств в процессах окислительной деструкции метилового оранжевого в присутствии пероксида водорода.
Материалы и методы исследования
Для формирования композиционного материала TiO2/Fe1,92Ti0,61O4/Fe2O3 была использована методика, подробно описанная в [2]. В качестве исходных веществ были использованы оксид титана (IV), соль Мора (NH4)2Fe(SO4)2·12H2O квалификации хч, водные растворы аммиака (NH3·H2O) с концентрацией 25 % (масс.) и лимонной кислоты (C6H8O7) с концентрацией 6,25 моль/л. Исходные вещества помещали в стальной реакционный сосуд и подвергали термообработке до полного разложения органической составляющей. Фазовый состав изучали на рентгеновском дифрактометре ARL X’TRA (использовали Cu-Kα излучение) в НИИ Нанотехнологий и новых материалов ЦКП «Нанотехнологии» ЮРГПУ (НПИ). При анализе количественного соотношения между фазами использовали методику, описанную в [3, 5]. Определение площади поверхности проводили на аппарате ChemiSorb 2750 В в НИИ Нанотехнологий и новых материалов ЦКП «Нанотехнологии» ЮРГПУ (НПИ).
Расчет среднего размера кристаллитов проводили по методу Шеррера по линии 311 по формуле
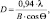
где D – средний размер кристаллов, нм; λ – длина волны рентгеновского излучения, нм; B – значение ширины линии пика на половине его высоты; cos θ – значение косинуса угла для пика.
Изучение каталитической активности синтезированных материалов проводили на модельном растворе метилового оранжевого с концентрацией 40 мг/л. При этом 10 мл исходного раствора метилового оранжевого помещали в плоскодонную колбу, добавляли 0,0010 г катализатора и 2 мл раствора пероксида водорода с концентрацией 3 % (масс.). Определение концентрации метилового оранжевого в растворе проводили фотокалориметрическим методом с помощью прибора КФК-2-УХЛ 4,2 через определенные интервалы времени. Расчет количества метилового оранжевого, подвергшегося каталитической деструкции (Р), проводили по формуле
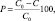
где С0 – начальная концентрация раствора, мг/л; С – текущее значение концентрации раствора, мг/л.
Результаты исследования и их обсуждение
Синтез материала проводили по следующей методике. Навеску оксида титана (IV) и соли Мора тщательно гомогенизировали, помещали в реакционный сосуд из нержавеющей стали, добавляли при интенсивном перемешивании водный раствор аммиака и затем – раствор лимонной кислоты. В результате наблюдали образование суспензии серого цвета, а затем – бежевого с зеленоватым оттенком. Полученный прекурсор нагревали при перемешивании до полного испарения жидкости. При этом происходило образование вязкого желто-зеленого гелеобразного вещества, переходившего постепенно в твердый пористый материал. Нагревание продолжали до полного разложения органической составляющей. При этом происходил процесс интенсивной деструкции материала, сопровождающийся выделением газообразных веществ и свечением реакционной системы. Полученный красно-коричневый порошок имел пористую структуру. Рентгенограмма синтезированного материала приведена на рис. 1. На рентгенограмме образца можно выделить линии, характеризующие фазы гематита Fe2O3 (PGF Number 010-85-0599), анатаза TiO2 (PGF Number 010-79-6031 и 010-75-2547) и твердого раствора состава Fe(Fe0,92Ti0,61)O4 (PGF Number 019-71-6450) со структурой кубической шпинели.
Формирование структуры образца может протекать по следующему механизму. В водном растворе соль Мора диссоциирует по схеме
(NH4)2Fe(SO4)2·= 2NH4+ + Fe2+ + 2SO42–.
В присутствии раствора аммиака образуется осадок гидроксида железа (II):
Fe2+ + 2OH– = Fe(OH)2,
который частично окисляется кислородом воздуха
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3.
Некоторое количество осадков гидроксидов адсорбируется на поверхности оксида титана (IV). При введении в реакционную систему лимонной кислоты происходит нейтрализация гидроксидов, имеющихся в растворе
Fe(OH)3 + C6H8O7 = Fe(C6H5O7) + 3H2O
с формированием хелатных комплексов
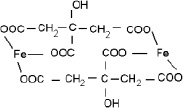
с участием катионов железа. При последующем нагревании происходит разложение комплексов с образованием дисперсного порошка оксида Fe2O3.
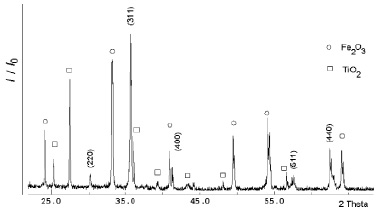
Рис. 1. Рентгенограмма образца состава TiO2/Fe1,92Ti0,61O4/Fe2O3. Индексированы линии, принадлежащие шпинели
Гидроксиды железа, закрепленные на поверхности TiO2, разлагаются с образованием твердого раствора по схемам
2Fe(OH)2 + TiO2 = Fe2TiO4 + 2H2O;
1,9Fe(OH)3 + 0,575TiO2 = Fe1,72Ti0,51O4 + 2,85H2O.
Образующийся материал имеет вид рыхлого пористого порошка. Средний размер зерен кристаллов, рассчитанный по формуле Шеррера, несколько выше значений для хорошо окристаллизованных материалов и составляет 8,42 нм. Площадь поверхности, измеренная методом ВЕТ, равна 6 м2/г.
Изучение каталитической активности синтезированных материалов проводили на примере реакции окислительной деструкции метилового оранжевого в присутствии пероксида водорода. В ходе проведенного исследования установлено, что композитный материал состава TiO2/Fe1,92Ti0,61O4/Fe2O3 проявляет высокую каталитическую активность в реакции Фентона. Временная зависимость количества метилового оранжевого, подвергшегося каталитической деструкции, приведена на рис. 2. Для сравнения на рис. 2 приведены также данные для характеристики каталитических свойств оксида титана (IV). Как видно из рис. 2, тип зависимости для TiO2 имеет вид, характерный для адсорбции молекул непористым твердым телом. Зависимость для синтезированного композиционного материала имеет вид S-образной кривой, характерной для мезопористого твердого вещества. Относительно невысокая скорость реакции в начальный период времени может быть связана с повышенной кристалличностью материала и вследствие этого малым количеством активных центров.
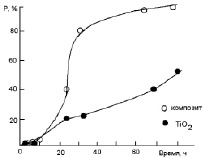
Рис. 2. Зависимость степени разложения метилового оранжевого в присутствии катализаторов от времени протекания реакции
Согласно результатам проведенного исследования, в случае применения композиционного материала TiO2/Fe1,92Ti0,61O4/Fe2O3 в процессе окислительной деструкции метилового оранжевого в присутствии пероксида водорода удается достичь практически полного удаления органического вещества из водного раствора. Полученные результаты могут служить ориентиром для выбора материалов, перспективных для применения в системах очистки сточных вод промышленных предприятий, использующих в производственных циклах органические красители.
Выводы
Изучен процесс фазообразования в системе состава TiO2/Fe1,92Ti0,61O4/Fe2O3. Предложен механизм формирования структуры материала, который включает стадию образования гидроксида железа (II), его частичное окисление кислородом воздуха до Fe(OH)3 с последующим закреплением некоторого количества гидроксидов на поверхности TiO2. Установлена высокая каталитическая активность синтезированных материалов в процессе окислительной деструкции метилового оранжевого в присутствии пероксида водорода, что может быть полезным для разработки материалов для очистки сточных вод промышленных предприятий, использующих в производственных циклах органические красители.
Рецензенты:
Таланов В.М., д.х.н., профессор кафедры «Общая химия и технология силикатов», ФГБОУ ВПО «Южно-Российский государственный политехнический университет имени М.И. Платова», г. Новочеркасск;
Балакай В.И., д.т.н., профессор, декан технологического факультета, ФГБОУ ВПО «Южно-Российский государственный политехнический университет имени М.И. Платова», г. Новочеркасск.



