За последнее десятилетие в литературе появилось много новых сведений о ценных свойствах органических соединений теллура, и интерес исследователей всего мира к этому разделу химии существенно возрос [1–3]. Высокая биологическая активность обнаружена у ряда новых органических производных теллура [3–5].
На базе четыреххлористого теллура синтезированы препараты с высокой противораковой и антивирусной активностью [3–5]. В связи с этими новыми данными синтез ранее неизвестных органических производных теллура на основе тетрагалогенидов теллура вызывает большой интерес ученых.
Известный теллурсодержащий препарат AS101, полученный из четыреххлористого теллура и этиленгликоля, после прохождения клинических испытаний был рекомендован для лечения больных раком (в сочетании с противоопухолевыми препаратами), а также больных псориазом [3].
В современном органическом синтезе теллурорганические вещества широко используются в качестве исходных соединений и синтонов. В частности, они применяются в стереоселективном синтезе функциональных алкенов. Присоединение четыреххлористого теллура к ацетиленами протекает регио- и стереоселективно; последующие реакции кросс-сочетания или переметаллирования образовавшегося аддукта с заменой теллурсодержащих групп на органические функции приводят к функциональным алкенам заданной стереоконфигурации [6, 7].
С целью получения препаратов с практически важными свойствами нами систематически изучаются реакции четырехбромистого и четыреххлористого теллура с непредельными веществами [8–10]. Нами впервые разработаны процессы алкоксителлурирования алкенов четырехбромистым теллуром, которые приводят к алкоксилированным алкилтрибромтелланам с высоким выходом [8–10]. Следует подчеркнуть, что четыреххлористый теллур не следует применять в реакциях алкоксителлурирования в среде спиртов, так как в этих условиях идет алкоголиз связи теллур–хлор.
Данные о реакции пропоксителлурирования в литературе отсутствуют.
Цель исследования: разработка технологичных региоселективных методов синтеза ранее неизвестных трихлор(2-пропоксиалкил)телланов и трибром(2-пропоксиалкил)телланов на основе систематических исследований реакций пропоксителлурирования 1-алкенов тетрагалогенидами теллура.
Материалы и методы исследования
Спектры ЯМР 1Н и 13С снимали на спектрометре Bruker DPX-400 на рабочих частотах 400,13 и 100,61 МГц соответственно в ДМСО-d6, внутренний стандарт – ГМДС. Для элементного анализа использован прибор Thermo Finigan EA 1112. В реакциях использовались осушенные и перегнанные растворители.
Трибром(2-пропоксигексил)теллан (4). К смеси 0,894 г (2 ммоль) четырехбромистого теллура и 25 мл пропилового спирта добавляли по каплям раствор 0,168 г (2 ммоль) 1-гекcена в 5 мл пропилового спирта в течение 5 мин. Реакционную смесь перемешивали 1 ч при комнатной температуре и 7 ч при температуре 65–75 °С, фильтровали. Растворитель удаляли на роторном испарителе, остаток сушили в вакууме. Выход: 0,858 г (84 %), темно-желтое вещество.
Спектр ЯМР 1Н, δ, м.д.: 0,96 т (3Н, СН3), 1,21 т (3Н, СН3), 1,29–1,39 м (2Н, СН2), 1,68–1.80 м (4Н, СН2), 1,89–1,94 м (2Н, СН2), 3,25–3,34 м (2H, ОСН2), 4,35–4,43 м (1Н, ОСН), 4,58–4,70 м (2H, ТеСН2). Спектр ЯМР 13С, δ, м.д.: 13,9 (CH3), 14,2 (CH3), 22,0 (CH2), 28,7 (CH2), 31,2 (CH2), 34,2 (CH2), 60,7 (Br3TeСH2), 66,7 (OCH2), 79,8 (OCH). Найдено, %: С 20,89; Н 3,92; Br 47,23; Te 25,28, C9H19Br3ОTe. Вычислено, %: С 21,17; Н 3,75; Br 46,95; Te 24,99.
Трибром(2-пропоксигептил)теллан (5). К смеси 0,894 г (2 ммоль) четырехбромистого теллура и 30 мл пропилового спирта добавляли по каплям раствор 0,196 г (2 ммоль) 1-гептена в 5 мл пропилового спирта в течение 5 мин. Реакционную смесь перемешивали 1 ч при комнатной температуре и 8 ч при температуре 65–75оС, фильтровали. Растворитель удаляли на роторном испарителе, остаток сушили в вакууме. Выход: 0,86 г (82 %), темно-желтое вещество.
Спектр ЯМР 1Н, δ, м.д.: 0,98 т (3Н, СН3), 1,18 т (3Н, СН3), 1,25–1,50 м (6Н, СН2), 1,69–1,78 м (2Н, СН2), 1,91–1,98 м (2Н, СН2), 3,27–3,34 м (2H, ОСН2), 4,32–4,42 м (1Н, ОСН), 4,54–4,68 м (2H ТеСН2). Спектр ЯМР 13С, δ, м.д.: 13,9 (CH3), 14,1 (CH3), 22,1 (CH2), 24,4 (CH2), 28,7 (CH2), 31,8 (CH2), 34,2 (CH2), 60,8 (Br3TeСH2), 69,7 (OCH2), 79,8 (OCH). Найдено, %: С 23,17; Н 3,86; Br 46,01; Te 24,59. C10H21Br3ОTe. Вычислено, %: С 22,90; Н 4,03; Br 45,70; Te 24,32.
Трихлор(2-пропоксиоктил)теллан (6). К смеси 0,894 г (2 ммоль) четырехбромистого теллура и 30 мл пропилового спирта добавляли по каплям раствор 0,224 г (2 ммоль) 1-октена в 5 мл пропилового спирта в течение 10 мин. Реакционную смесь перемешивали 10 ч при температуре 65–75оС, фильтровали. Растворитель удаляли на роторном испарителе, остаток сушили в вакууме. Выход 0,862 г (80 %), темно-желтое вещество.
Спектр ЯМР 1Н, δ, м.д.: 0,96 т (3Н, СН3), 1,21 т (3Н, СН3), 1,23–1,55 м (10Н, СН2), 1,54–1,62 м (2Н, СН2), 3,26–3,34 м (2H, ОСН2), 4,33–4,42 м (1Н, ОСН), 4,53–4,67 м (2H ТеСН2). Спектр ЯМР 13С, δ, м.д.: 14,1 (CH3), 14,3 (CH3), 23,4 (CH2), 25,3 (CH2), 28,1 (CH2), 29,5 (CH2), 31,4 (CH2), 33,2 (CH2), 60,5 (Br3TeСH2), 64,7 (OCH2), 78,9 (OCH). Найдено, %: С 24,28; Н 4,12; Br 44,81; Te 23,94. C11H23Br3ОTe. Вычислено, %: С 24,53; Н 4,30; Br 44,51; Te 23,69.
Однореакторный метод синтеза трихлор(2-пропоксиалкил)телланов 7–9. Трихлор(2-пропоксигексил)теллан (7). К охлажденной на ледяной бане до 0–3 °С смеси 0,539 г (2 ммоль) четыреххлористого теллура и 15 мл хлороформа добавляли по каплям раствор 0,168 г (2 ммоль) 1-гекcена в 5 мл хлороформа и перемешивали реакционную смесь 2 ч при 0–3 °С и 18 ч при комнатной температуре. К полученной смеси с образовавшимся трихлор(2-хлоргексил)телланом добавили 5 мл пропанола и нагревали реакционную смесь до кипения в течение 8 ч. Смесь фильтровали, растворитель удаляли на роторном испарителе, остаток сушили в вакууме. Выход: 0,679 г (90 %), темно-серое вещество.
Спектр ЯМР 1Н, δ, м.д.: 1,01 т (3H, CH3), 1,25 т (3H, CH3), 1,32–1,56 м (6H, CH2), 1,79–1,97 м (2H, CH2), 3,85–3,93 м (1H, OCH2), 3,93–4,03 м (1H, OCH2), 4,42–4,50 м (2H, Cl3TeCH2), 4,55–4,68 м (1H, OCH). Спектр ЯМР 13С, δ, м.д.: 14,3 (CH3), 15,5 (CH3), 22,6 (CH2), 25,4 (CH2), 29,3 (CH2), 34,4 (CH2), 66,1 (OCH2), 67,5 (Cl3TeCH2), 76,4 (OCH). Найдено, %: С 28,38; Н 4,89; Cl 27,98; Te 34,12. C9H19Cl3ОTe. Вычислено, %: С 28,66; Н 5,08; Cl 28,20; Te 33,83.
Трихлор(2-пропоксигептил)теллан (8). К охлажденной на ледяной бане до 0–3 °С смеси 0,539 г (2 ммоль) четыреххлористого теллура и 18 мл хлороформа добавляли по каплям раствор 0,196 г (2 ммоль) 1-гептена в 6 мл хлороформа и перемешивали реакционную смесь 3 ч при 0–3 °С и 20 ч при комнатной температуре. К полученной смеси с образовавшимся трихлор(2-хлоргептил)телланом добавили 6 мл пропанола и нагревали реакционную смесь до кипения в течение 9 ч. Смесь фильтровали, растворитель удаляли на роторном испарителе, остаток сушили в вакууме. Выход 0,681 г (87 %), темно-серое вещество.
Спектр ЯМР 1Н, δ, м.д.: 0,98 т (3H, CH3), 1,21 т (3H, CH3), 1,31–1,58 м (8H, CH2), 1,80–1,98 м (2H, CH2), 3,82–3,93 м (1H, OCH2), 3,92–4,03 м (1H, OCH2), 4,40–4,49 м (2H, Cl3TeCH2), 4,53–4,65 м (1H, OCH). Спектр ЯМР 13С, δ, м.д.: 14,1 (CH3), 15,3 (CH3), 22,3 (CH2), 25,8 (CH2), 29,3 (CH2), 31,4 (CH2), 34,1 (CH2), 66,1 (OCH2), 67,6 (Cl3TeCH2), 76,5 (OCH). Найдено, %: С 30,42; Н 5,23; Cl 26,90; Te 32,34. C10H21Cl3ОTe. Вычислено, %: С 30,70; Н 5,41; Cl 27,19; Te 32,61.
Трихлор(2-пропоксиоктил)теллан (8). К охлажденной на ледяной бане до 0–3 °С смеси 0,539 г (2 ммоль) четыреххлористого теллура и 16 мл хлороформа добавляли по каплям раствор 0,224 г (2 ммоль) 1-октена в 8 мл хлороформа и перемешивали реакционную смесь 3 ч при 0–3 °С и 24 ч при комнатной температуре. К полученной смеси с образовавшимся трихлор(2-хлороктил)телланом добавили 6 мл пропанола и нагревали реакционную смесь до кипения в течение 10 ч. Смесь фильтровали, растворитель удаляли на роторном испарителе, остаток сушили в вакууме. Выход 0,689 г (85 %), темно-серое вещество.
Спектр ЯМР 1Н, δ, м.д.: 0,96 т (3H, CH3), 1,19 т (3H, CH3), 1,23–1,58 м (10H, CH2), 1,83–1,98 м (2H, CH2), 3,83–3,92 м (1H, OCH2), 3,94–4–03 м (1H, OCH2), 4,38–4,48 м (2H, Cl3TeCH2), 4,52–4,63 м (1H, OCH). Спектр ЯМР 13С, δ, м.д.: 14,1 (CH3), 15,2 (CH3), 22,4 (CH2), 25,6 (CH2), 28,1 (CH2), 29,7 (CH2), 31,6 (CH2), 34,2 (CH2), 66,2 (OCH2), 67,7 (Cl3TeCH2), 76,7 (OCH). Найдено, %: С 32,31; Н 5,92; Cl 26,54; Te 31,73. C11H23Cl3ОTe. Вычислено, %: С 32,60; Н 5,72; Cl 26,24; Te 31,49.
Реакция пропоксителлурирования 1-алкенов тетрахлоридом теллура. К смеси 0,539 г (2 ммоль) четыреххлористого теллура и 20 мл хлороформа добавляли по каплям раствор 0,168 г (2 ммоль) 1-гексена в 5 мл пропанола в течение 5 мин. Реакционную смесь нагревали до кипения в течение 8 ч. Смесь фильтровали, растворитель удаляли на роторном испарителе, остаток сушили в вакууме. Выход 0,604 г (80 %) теллана 7, темно-серое вещество с чистотой около 94 % (данные ЯМР).
В аналогичных условиях были из четыреххлористого теллура и 1-алкенов получены теллан 8 с выходом 77 % (чистота около 92 % по данным ЯМР) и теллан 9 с выходом 72 % (чистота около 90 % по данным ЯМР).
Результаты исследования и их обсуждение
Пропоксителлурирование не описано в литературе.
Мы впервые реализовали и систематически исследовали процессы пропоксителлурирования ненасыщенных субстратов 1–3 четырехбромистым и четыреххлористым теллуром.
Процесс пропоксителлурирования взаимодействием четырехбромистого теллура с ненасыщенными субстратами 1–3 в пропаноле приводит к ранее неизвестным трибром(2-пропоксиалкил)телланам 4–6 с выходами 80–84 % (схема 1).
В условиях процесса связь Te-Br в четырехбромистом теллуре не подвергается алкоголизу.
Реакция пропоксителлурирования тетрахлоридом теллура не может быть проведена в пропаноле, поскольку в этих условиях TeCl4 подвергается алкоголизу связи теллур–хлор. Реакция пропоксителлурирования алкенов 1–3 осуществлена в смеси растворителей пропанол – хлороформ (объемное соотношение 1:4) при нагревании до кипения хлороформа (схема 2). Выход полученных таким путем трихлор(2-пропоксиалкил)телланов 7–9 составил 72–80 % при чистоте около 90–94 % (данные ЯМР).
Следует отметить, что трихлор(2-этоксиалкил)телланы, полученные нами ранее в аналогичных условиях реакцией этоксителлурирования алкенов 1–3 тетрахлоридом теллура в смеси растворителей этанол – хлороформ, также имели недостаточно высокую чистоту [10].
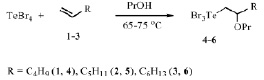
Схема 1. Реакция пропоксителлурирования алкенов тетрабромидом теллура

Схема 2. Реакция пропоксителлурирования алкенов тетрахлоридом теллура
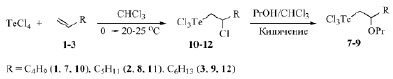
Схема 3. Селективный метод синтеза трихлор(2-пропоксиалкил)телланов 7–9
Более селективным способом получения телланов 7–9 оказался подход, основанный на реакции нуклеофильного замещения атома хлора на пропоксигруппу в трихлор(2-хлоралкил)телланах 10–12. Ранее соединения 10–12 получены нами присоединением четыреххлористого теллура к алкенам 1–3 [9].
Для селективного синтеза телланов 7–9 разработан эффективный однореакторный метод на основе четыреххлористого теллура, алкенов 1–3 и пропанола без выделения промежуточных трихлор(2-хлоралкил)телланов 10–12. После получения соединений 10–12 в хлороформе к реакционной смеси добавляют пропанол и нагревают смесь до кипения в течение 8–10 ч. Этим методом удается получить трихлор(2-пропоксиалкил)телланы 7–9 с выходом 85–90 % и высокой степенью чистоты (схема 3).
Легкость нуклеофильного замещения атома хлора в телланах 10–12, по-видимому, обусловлена наличием сильной электроноакцепторной трихлортелланильной группы.
Структуры синтезированных соединений доказаны методами ядерного магнитного резонанса на ядрах 1Н и 13С, их состав подтвержден данными элементного анализа. Как следует из анализа спектральных данных, присоединение атома теллура происходит к терминальному углеродному атому двойной связи с образованием продуктов по правилу Марковникова. Наблюдаемые в спектрах ЯМР 13С синтезированных соединений 4–7 высокие значения химических сдвигов sp3-гибридизованного атома углерода групп CH2TeBr3 (60,5–60,8 м.д.) и CH2TeCl3 (67,5–67,7 м.д.) указывают на сильный электроноакцепторный эффект тригалогентелланильных заместителей. Подобные значения сигналов групп CH2TeBr3 и CH2TeCl3 наблюдались нами в спектрах ядерного магнитного резонанса на ядрах 1Н и 13С близких по строению продуктов: трихлор(2-метоксиалкил)телланов, трибром(2-метоксиалкил)телланов, трихлор(2-этоксиалкил)телланов и трибром(2-этоксиалкил)телланов [8–10].
Выводы
Впервые осуществлен процесс пропоксителлурирования ненасыщенных субстратов четырехбромистым и четыреххлористым теллуром. Процесс прост в техническом оформлении и технологичен. На основе четырехбромистого и четыреххлористого теллура и алкенов 1–3 разработаны технологичные региоселективные методы синтеза ранее неизвестных трибром(2-пропоксиалкил)телланов 4–6 и трихлор(2-пропоксиалкил)телланов 7–9 – перспективных реагентов для микро- и наноэлектроники, полупродуктов для элементоорганического синтеза.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований (проект № 16-33-60199_мол_а_дк). Авторы благодарят Байкальский аналитический центр коллективного пользования Сибирского отделения Российской академии наук за спектральные и аналитические исследования.



