Под плевральным выпотом понимается патологическое скопление жидкости в полости плевры. В зависимости от биохимического и цитологического состава все плевральные выпоты делятся на транссудат и экссудат, последний отличается большей относительной плотностью (более 1,018), высоким содержанием белка (более 30 г/л), в том числе фибриногена, значительным количеством клеточных элементов. В зависимости от клеточного состава различают два основных вида экссудата – серозный и гнойный, и несколько их разновидностей [3].
Гнойный плеврит, или эмпиема плевры, характеризуется скоплением гноя в плевральной полости и чаще развивается вторично в результате распространения на плевру инфекционного процесса из лёгких. Выделение эмпиемы в самостоятельный вид воспаления плевры подчёркивает необходимость ранней диагностики и проведения интенсивного местного лечения, как правило, в условиях хирургического отделения.
Пиопневмотораксом называют тяжёлое гнойное воспаление в плевральной полости, когда в ней содержится не только гнойный экссудат, но и воздух, попавший туда из полости деструкции в лёгком. Лёгкое частично спадается, а через бронхоплевральную фистулу в полость плевры постоянно поступает воздух, в результате чего нагноительный процесс приобретает хроническое течение.
Традиционным методом диагностики плевральных выпотов является рентгенологический, однако с его помощью можно выявить жидкость объёмом не менее 100‒150 мл и нельзя оценить характер самого содержимого [1]. При УЗИ грудной клетки можно не только обнаружить плевральный выпот объёмом 5–10 мл, но и оценить его эхоструктуру, на основании которой сделать вывод о характере жидкости [2, 6]. Однако ультразвуковой диагностике именно гнойной патологии плевральной полости посвящены единичные работы, недостаточно освещены многие вопросы методики и дифференциальной диагностики эмпиемы и пиопневмоторакса [5, 7]. При этом в клинической практике УЗИ грудной клетки всё шире используется для визуализации различных патологических процессов в плевре, проводится стандартизация исследования [4]. Поэтому целью исследования являлось совершенствование методики УЗИ плевральных выпотов и изучение эхосемиотики эмпиемы и пиопневмоторакса.
Материалы и методы исследования
УЗИ грудной клетки выполнено 285 пациентам, госпитализированным в отделение торакальной хирургии ГКБ № 5 г. Нижнего Новгорода с гнойными плевральными выпотами, из них 220 больных эмпиемой плевры и 65 – с пиопневмотораксом. Исследование проводилось на сканере среднего класса SIM 7000 (Еsaote, Италия) механическими секторными датчиками 3,5 и 7,5 МГц и верифицировано результатами торакальных пункций с микробиологическим анализом пунктата.
При УЗИ грудной клетки воздушная лёгочная ткань не препятствует визуализации содержимого плевральной полости, и его можно детально осмотреть из межреберий. Хорошие акустические свойства жидкости и возможность сканирования на всю её глубину создают условия для детального изучения эхоструктуры и пространственной конфигурации плевральных выпотов.
Пациента обследовали в вертикальном положении, сначала выполняли сканирование одной половины грудной клетки, потом другой, в направлении снизу вверх последовательно по задней, боковой и передней поверхности. Исследование начинали со спины с проекции заднего рёберно-диафрагмального синуса плевры, то есть с места наиболее вероятного местонахождения жидкости в самой низкой точке плевральной полости. Датчик устанавливали в продольной плоскости в X или XI межреберье по лопаточной линии и сканировали плевральный синус на всём протяжении. В норме синус не содержал жидкость и как таковой не визуализировался. Он определялся условно как пространство, в которое на вдохе проникал нижний край лёгкого, смещаясь вниз вдоль грудной стенки до пристеночного участка диафрагмы, где она под острым углом переходила в грудную стенку.
Затем перемещали датчик латерально по межреберью, плавно покачивая его в вертикальной плоскости и осматривая боковые отделы, и заканчивали визуализацией переднего синуса по парастернальной линии, для чего датчик устанавливали субкостально или в межреберье над местом прикрепления рёберной дуги к грудине. Периодически датчик поворачивали на 90º по часовой стрелке и проводили поперечное сканирование, также сочетая его с покачиванием датчика, но в горизонтальной плоскости.
Межрёберное сканирование верхних отделов грудной клетки проводили спереди из II–IV межреберий с опущенной рукой. При осмотре аксиллярной области пациент максимально поднимал руку вверх и немного наклонялся в противоположную сторону, обеспечивая широкий доступ к подмышечной области. Визуализацию верхних отделов сзади проводили с отведением лопатки, для чего пациент клал руку на противоположное плечо, отводя лопатку вперёд и в сторону.
При определении места плевральной пункции или дренирования в межреберье маркером отмечали центр выпота или несколько ниже при условии, что там нет лёгкого или внутриплевральных эхогенных структур, которые могли препятствовать ходу иглы. Это позволяло максимально обезопасить процедуру и повысить её эффективность. У тяжёлых пациентов исследование выполняли в горизонтальном положении, поворачивая больного на бок, и метку ставили в том положении, в котором будет проводиться пункция.
Результаты исследования и их обсуждение
Главным ультразвуковым признаком эмпиемы плевры являлась крупнозернистая неоднородная взвесь с высокой плотностью частиц в единице объёма, которая придавала выпоту достаточно высокую эхогенность, иногда даже превышавшую эхогенность нормальной печени (рис. 1). Она выявлена у 264 (92,6 %) больных, значительно реже при эмпиеме наблюдалась относительно рыхлая, мелкозернистая и однородная взвесь. Ещё одним отличием гнойной взвеси являлась малая подвижность её частиц, которые незначительно смещались при сердцебиении или интенсивных глубоких вдохах.
Это свойственно распространённой эмпиеме и крупным гнойным осумкованиям, но в небольших осумкованных полостях взвесь оставалась неподвижной. В большинстве случаев взвесь диффузно и равномерно занимала весь объём и только у 18 (6,3 %) больных её плотность и эхогенность нарастали в пристеночной области, что делало границу утолщенной плевры с гнойным содержимым менее чёткой и затрудняло точное определение толщины плевральных наложений.
При высокой плотности и эхогенности неподвижная гнойная взвесь по эхоструктуре напоминала печень при жировом гепатозе, а утолщенная плевра выглядела по сравнению с ней гипоэхогенной (рис. 2). Такая эхокартина возникала при густом сливкообразном гное, который в серошкальном изображении имитировал объёмное образование. Для дифференцировки с опухолью требовалось выявить смещение частиц взвеси при сердцебиении или форсированном дыхании. При разной консистенции гнойное содержимое приобретало неоднородную структуру с менее вязкими гипоэхогенными зонами, медленно менявшими конфигурацию при перемене положения тела пациента, а локальные скопления более густого гноя лоцировались в гипоэхогенном жидком содержимом как эхогенные опухолевидные объекты диаметром до 4–5 см.
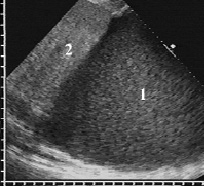
Рис. 1. Распространённая эмпиема плевры с плотной эхогенной взвесью (1), сопоставимой с эхогенностью нормальной печени (2)
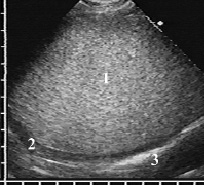
Рис. 2. Ограниченная эмпиема плевры с высоко эхогенной плотной однородной взвесью, имитировавшей солидное образование (1), гипоэхогенная утолщенная висцеральная плевра (2) вдоль гиперэхогенной границы воздушного лёгкого (3)
Равномерно утолщенная, с фибринозными наложениями плевра принципиально не отличалась от адгезивных изменений при экссудативном плеврите серозно-фибринозного характера. Стенки эмпиемной полости имели толщину до 5 мм, а при выраженных наложениях достигали 8 мм. Утолщенные листки плевры хорошо прослеживались вдоль грудной стенки, диафрагмы и лёгкого в виде дополнительной эхогенной полосы с чётким неровным контуром (рис. 3).
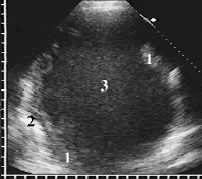
Рис. 3. Ограниченная эмпиема плевры. Утолщенная плевра в виде эхогенной полосы с чётким неровным контуром (1), отграничивающей гиперэхогенную поверхность воздушного лёгкого (2) от рыхлой мелкозернистой гнойной взвеси (3)
Изложенная эхокартина характерна для первично обследуемой полости эмпиемы. В процессе лечения после дренирования и промывания происходило значительное снижение плотности эхогенной взвеси, содержимое эмпиемного мешка становилось более однородным и анэхогенным, плевральные наложения уплотнялись. Размеры полости уменьшались, она приобретала более плоскую форму вдоль грудной стенки, а затем спадалась. В итоге на месте эмпиемы формировалась эхогенная шварта с облитерацией плевральной полости и отсутствием дыхательной подвижности лёгкого.
При пиопневмотораксе в плевральной полости содержался не только гнойный экссудат, но и воздух, как свободный, так и в виде отдельных мелких пузырьков в выпоте. Эхопризнаком пиопневмоторакса были множественные крупнозернистые и короткие линейные (длиной 2–3 мм) гиперэхогенные включения в виде очень яркой и крупной, но рыхлой взвеси, по своим размерам и эхогенности значительно превосходившей гнойную. Эти сигналы возникали при отражении ультразвука от мелких пузырьков воздуха, попавших в плевральную полость через бронхоплевральную фистулу при деструции в лёгком. Они диффузно распределялись по всему выпоту на фоне неоднородной гнойной взвеси или концентрировались в верхней части полости эмпиемы (рис. 4).
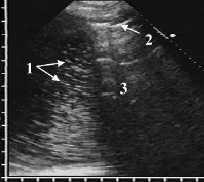
Рис. 4. Пиопневмоторакс: в плевральном выпоте видны множественные гиперэхогенные крупнозернистые и короткие линейные сигналы (1) от мелких пузырьков воздуха в гнойном экссудате, выше которых лоцируется гиперэхогенная линия (2) с дистальной акустической тенью (3) от свободного воздуха в плевральной полости
Вторым обязательным компонентом эхокартины при пиопневмотораксе являлся свободный воздух в плевральной полости. Скапливаясь выше неоднородного жидкого содержимого, он приводил к появлению над ним пристеночной гиперэхогенной линии, очень похожей на линию от поверхности воздушного лёгкого, но более интенсивной и с выраженными реверберациями «повторного эха». При неравномерной толщине плевральных наложений эта гиперэхогенная линия была неровной, ступенчатой, в точности повторяя внутренний рельеф утолщенной костальной плевры. Акустическая тень и дистальные реверберации позади неё перекрывали все глубже лежащие структуры. Вследствие передаточной пульсации при сердцебиении край этой линии смещался вверх-вниз вдоль грудной стенки с высокой частотой и небольшой амплитудой, напоминая движения иглы швейной машинки, в отличие от ритмичных дыхательных движений нижнего края лёгкого.
Отдельные гиперэхогенные включения воздуха, находившиеся во взвешенном состоянии в достаточно густом экссудате, имели незначительную смещаемость и колебались с небольшой амплитудой в такт с движениями сердца или лёгкого. Они оставались неподвижными только при плотной эхогенной гнойной взвеси. Часто мелкие гиперэхогенные сигналы скапливались у стенок полости эмпиемы, формируя вдоль них пунктирные белые линии или цепочки, подчёркивавшие поверхность утолщенной плевры. Мы назвали это симптомом подчёркивания, его лучше видно вдоль костальной и диафрагмальной плевры (рис. 5).
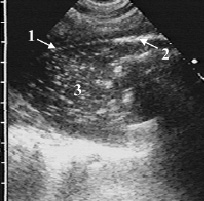
Рис. 5. Ограниченный пиопневмоторакс. В гнойном экссудате лоцируются гиперэхогенные крупнозернистые сигналы (1) от отдельных пузырьков воздуха, гиперэхогенная линия (2) с дистальной акустической тенью от свободного воздуха в плевральной полости, симптом подчёркивания – пристеночно мелкие пузырьки воздуха в виде цепочки гиперэхогенных сигналов вдоль внутренней поверхности утолщенной плевры (3)
Выводы
УЗИ грудной клетки является высоко информативным радиологически безопасным методом диагностики плевральных выпотов, который позволяет эргономично и неинвазивно установить гнойный характер экссудата и определить оптимальное место дренирования. Для эмпиемы плевры характерно наличие в экссудате неоднородной плотной малоподвижной эхогенной взвеси, выраженные плевральные наложения, частое осумкование. При пиопневмотораксе в структуре выпота лоцируются множественные рыхло расположенные крупнозернистые гиперэхогенные сигналы от мелких пузырьков воздуха в гнойном экссудате, выше которого видна гиперэхогенная пристеночная линия от свободного воздуха с акустической тенью и интенсивными реверберациями «повторного эха».
Рецензенты:Шарабрин Е.Г., д.м.н., профессор кафедры лучевой диагностики факультета повышения квалификации врачей, ГБОУ ВПО «Нижегородская государственная медицинская академия» Минздрава России, г. Нижний Новгород;
Казакова Л.В., д.м.н., заведующая отделением ультразвуковой диагностики, ФБУЗ «Приволжский окружной медицинский центр» ФМБА России, г. Нижний Новгород.
Работа поступила в редакцию 06.03.2015.



