Применение полимеров в фармацевтической технологии обусловило создание стоматологических пленок и гелей, обеспечивающих пролонгированное высвобождение лекарственных средств обезболивающего, антимикробного, противовоспалительного действия [8]. В результате совместных исследований кафедр фармацевтической технологии и микробиологии АГМУ в соответствии с принципами конструирования лекарственных препаратов для лечения заболеваний пародонта предложен состав экспериментального стоматологического геля, который получил условное название «Эстофит Дента». Действующими компонентами геля являются настойка календулы как противовоспалительное и антибактериальное средство и анестетик бензокаин. В качестве полимера-носителя в результате биофармацевтических исследований методом диализа выбран аквасорб А 380 [1, 5].
Определение фармацевтической доступности лекарственных препаратов по тесту «Растворение» традиционно используется при оценке качества пероральных лекарственных форм. Зарубежные фармакопеи предлагают использовать тест «Растворение» на приборе «лопасть над диском» для изучения кинетики высвобождения из пролонгированных лекарственных форм: трансдермальных пластырей и других трансдермальных систем, мазей, кремов и т.д. Принимая во внимание тот факт, что стоматологические гели должны обеспечивать пролонгированное высвобождение лекарственных веществ, изучение профилей высвобождения бензокаина из экспериментального препарата представляется актуальным. Другим требованием, которому должны отвечать стоматологические лекарственные препараты, является антимикробное действие в отношении широкого круга микроорганизмов, обитающих в ротовой полости.
Целью данной работы являлась изучение профилей высвобождения бензокаина на приборе «лопасть над диском» и оценка антимикробной активности стоматологического геля «Эстофит Дента».
Материалы и методы исследования
Высвобождение бензокаина из стоматологического геля «Эстофит Дента» изучали методом Transdermal delivery system на приборе «Лопасть над диском» [3, 6]. Навеску геля (1,0 г) помещали в экстракционную ячейку, диаметр поверхности которой составлял 44 мм, и на ячейку закрепляли полупроницаемую мембрану. Ячейку погружали в диализную среду и опускали лопастную мешалку так, чтобы между ячейкой и мешалкой расстояние составляло 25 ± 2 мм. В качестве акцепторной среды использовали воду очищенную или спирта этилового растворы в концентрации 10, 15, 20 и 30 % при температуре 37 ± 1 °С в объеме 500 мл. На предварительном этапе исследований было установлено, что целлофановая мембрана марки «Купрофан» в спирте этиловом растворе 10, 15, 20 и 30 % не теряет свойств полупроницаемости и не разрушается. Частота вращения лопасти составляла 50 об/мин. Отбор проб проводили через равные интервалы времени в объеме 5 мл, восполняя объем акцепторной средой. Оптическую плотность снимали на спектрофотометре Cary-50 при длине волны 284 нм (максимум поглощения бензокаина). Расчеты проводили с использованием определенного удельного показателя поглощения бензокаина при данной длине волны 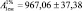 .
.
Антибактериальную активность стоматологического геля «Эстофит Дента» оценивали методом прямого контакта, который является модификацией метода серийных разведений, на 18 клинических штаммах микроорганизмов, выделенных от больных и хранящихся в музее кафедры микробиологии АГМУ. В эксперименте использованы штаммы Staphylococcus aureus 391, Staphylococcus aureus 392, Staphylococcus aureus 393, Staphylococcus epidermidis 486, Staphylococcus epidermidis 385, Staphylococcus epidermidis 387, Klebsiella 171, Klebsiella 172, Klebsiella 404, Echerichia coli 167, Echerichia coli 4711, Echerichia coli 4712, Candida 475, Candida 453, Candida 341, Candida 473, Candida 310, Candida 309, которые населяют полость рта в различные периоды жизни человека [4, 7, 9].
Методика микробиологических исследований заключалась в следующем: культуры тест-микробов выращивали 4 часа при температуре 37 ± 2 ° С на сахарном бульоне. Исходная посевная доза составляла 50 млн микробных клеток суточной агаровой культуры. Далее 0,1 мл четырехчасовой бульонной культуры тест-микроба вносили в 1 мл исследуемого геля и параллельно в 1 мл натрия хлорида раствор 0,9 % (контрольный опыт). Оптимальное время контакта микроорганизмов с изучаемым экспериментальным препаратом и в контроле составляло 3 и 24 часа. После контакта микроорганизмов с гелем «Эстофит Дента» и изотоническим раствором проводили посевы по 0,1 мл на поверхность мясопептонного агара в виде сплошного газона. Посевы инкубировали в термостате при температуре 37 ± 2 °С в течение 24 часов. Рост культур в результате посевов контрольного опыта принимали за 100 % [2].
Статистическую обработку экспериментальных данных осуществляли с использованием программ Statistica 6.1 и Microsoft Excel. Результаты исследований (Р = 95 %) обрабатывали при помощи критерия Стьюдента по стандартным методикам ГФ XII изд.
Результаты исследования и их обсуждение
Кинетические кривые высвобождения бензокаина из стоматологического геля «Эстофит Дента» на приборе «лопасть над диском» в различные диализные среды представлены на рис. 1.
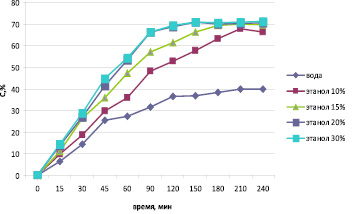
Рис. 1. Кинетические кривые высвобождения бензокаинаиз геля «Эстофит»Дента» на приборе «лопасть над диском»
Кинетические кривые, представленные на рис. 1, свидетельствуют о пролонгированном характере высвобождения бензокаина из стоматологического геля «Эстофит Дента». При использовании в качестве среды высвобождения воды очищенной из исследуемого препарата высвобождается за 45 мин 25,54 ± 1,39 %, за 2 часа 36,37 ± 1,11 %,за 3 часа 38,45 ± 2,45 % бензокаина. Сравнительный анализ профилей высвобождения бензокаина в воду очищенную и спирта этилового растворы 10–30 % позволяет сделать вывод о том, что введение этанола в состав акцепторной среды увеличивает высвобождение лекарственного вещества. Через 45 мин от начала эксперимента в диализную среду с добавлением 10 % этанола высвобождается 29,67 ± 1,29 %, 15 % этанола – 36,00 ± 1,08 %, 20 % этанола – 41,32 ± 0,45 %, 30 % этанола – 44,76 ± 0,63 % бензокаина соответственно. Более 70 % бензокаина высвобождается из геля «Эстофит Дента» в акцепторную среду с добавлением 30 % этанола через 2 часа, 20 % этанола через 3 часа от начала эксперимента. Таким образом, при изучении профилей растворения бензокаина из стоматологического геля «Эстофит Дента» рационально часть акцепторной среды замещать этанолом.
Результаты микробиологических исследований свидетельствуют о том, что через 3 часа после контакта изучаемого геля с суспензией Staphylococcus aureus и последующего посева на мясопептонный агар наблюдался рост единичных колоний микроорганизмов, представленных Staphylococcus aureus 392. После двадцатичетырехчасового контакта с гелем рост всех культур Staphylococcus aureus подавлялся полностью, при этом при посеве контролей (натрия хлорида раствор 0,9 %) как после 3 часов, так и после 24 часов контакта наблюдался обильный рост стафилококков (> 104). Подавление роста штаммов Staphylococcus aureus, используемых в эксперименте, оценивается на 99,9 % через 3 часа и 100 % через 24 часа прямого контакта (рис. 2). Рост Staphylococcus epidermidis полностью подавлялся экспериментальным препаратом как через 3 часа, так и через 24 часа прямого контакта, в контролях количество колоний превышало 104.
Грамотрицательные Klebsiella pneumonia относятся к условно-патогенным микроорганизмам, входят в состав нормальной микрофлоры носоглотки и верхних дыхательных путей и могут в норме обнаруживаться на слизистой полости рта, при снижении иммунитета могут принимать участие в патологических процессах полости рта [7]. После внесения суспензий Klebsiella pneumonia в гель «Эстофит Дента» наблюдался рост единичных колоний штаммов Klebsiella 172 и Klebsiella 404: 2 и 4 колонии после трехчасового контакта и 2 и 1 колонии после 24 часов контакта соответственно. Антибактериальная активность геля «Эстофит Дента» методом прямого контакта в отношении Klebsiella pneumonia составляет 99,9 %.
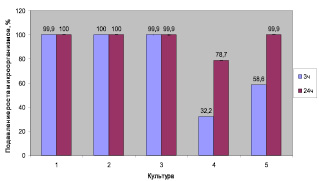
Рис. 2. Подавление роста микроорганизмов экспериментальным препаратом«Эстофит Дента» (метод прямого контакта):1 – Staphylococcus aureus, 2 – Staphylococcus epidermidis, 3 – Klebsiella, 4 – Echerichia coli, 5 – Candida
Кишечная палочка является представителем транзиторной (случайной) микрофлоры, тем не менее этот условно-патогенный микроорганизм в некоторых случаях, преимущественно у пожилых людей, может принимать участие в патологических процессах полости рта [7]. Через 3 часа инкубации было выявлено подавление исследуемым составом роста только одного штамма Echerichia coli 167, при этом на агаре наблюдался рост 336 колоний. Другие используемые в эксперименте штаммы обильно росли после 3 часов контакта с исследуемым гелем. Через 24 часа после внесения в гели суспензий Echerichia coli наблюдался рост колоний при высеве всех штаммов, но рост был существенно меньше, чем в контроле (2840 и более 104 колоний соответственно). Обобщение полученных данных позволило сделать следующий вывод: антибактериальная активность экспериментального геля «Эстофит Дента» в отношении Echerichia coli методом прямого контакта составляет 32,2 % через 3 часа, 78,7 % ‒ через 24 часа инкубации.
Candida albicans – это условно-патогенный микроорганизм, который часто вызывает поражение слизистой полости рта, особенно у грудных детей, а также у пожилых людей, носящих зубные протезы [7]. Антибактериальные свойства экспериментального препарата «Эстофит Дента» определяли по отношению к 6 штаммам Candida albicans, при этом в отношении 4 штаммов Candida albicans (341, 473, 310, 309) была выявлена выраженная антибактериальная активность. Через 3 часа контакта суспензии Candida albicans с экспериментальным препаратом рост микроорганизмов практически полностью отсутствовал, в то время как в контролях наблюдался обильный рост колоний. Через 24 часа контакта суспензии указанных микробов с испытуемым гелем рост дрожжеподобных грибов рода Candida также практически полностью отсутствовал, наблюдался рост 3 колоний на агаре штамма Candida albicans 475, в контролях с натрия хлоридом раствором изотоническим наблюдался обильный рост. Суммарная антимикробная активность экспериментального стоматологического геля «Эстофит Дента» в отношении Candida albicans составляет 58,6 % через 3 часа и 99,9 % через 24 часа прямого контакта.
Заключение
В результате проведенных исследований установлено, что стоматологический гель «Эстофит Дента» обеспечивает пролонгированное высвобождение бензокаина и проявляет выраженный антимикробный эффект в отношении клинических штаммов грампозитивных микроорганизмов: коагулазоположительных Staphylococcus aureus, коагулазоотрицательных Staphylococcus epidermidis; грамнегативных палочек Klebsiella pneumonia; дрожжеподобных грибов Candida albicans; умеренное антибактериальное действие в отношении Echerichia coli.
Рецензенты:
Лампатов В.В., д.б.н., профессор кафедры фармакологии, ГБОУ ВПО «Алтайский государственный медицинский университет» Минздрава России, г. Барнаул;
Федосеева Л.М., д.фарм.н., профессор, зав. кафедрой фармацевтической химии с курсом органической и токсикологической химии, ГБОУ ВПО «Алтайский государственный медицинский университет» Минздрава России, г. Барнаул.
Работа поступила в редакцию 19.07.2013.



